��Ŀ����
��1L������ͨ��CO2��H2��2mol����һ�������·�����Ӧ��CO2+H2?CO+H2O���ش��������⣺
��1����830�������£���Ӧ�ﵽƽ��ʱCO2��ת����Ϊ50%�����������ƽ�ⳣ��K1= ��
��2���ڣ�1���Ļ����ϣ�����ϵ�¶Ƚ���800�森��֪�������µ�ƽ�ⳣ��K2=0.81��������֪�÷�Ӧ������ӦΪ ��Ӧ������ȡ��������ȡ�����
��3���ڣ�1���Ļ����ϣ�ѹ���������֮0.5L���������µ�ƽ�ⳣ��ΪK3����K3 K1
��4��830��ʱ��ijʱ�̲����ϵ�и����ʵ������£�n��CO2��=1.2mol��n��H2��=1.5mol��
n��CO��=0.9mol��n��H2O��=0.9mol�����ʱ�÷�Ӧ ���У�
���������Ӧ�������淴Ӧ������ƽ��״̬������
��1����830�������£���Ӧ�ﵽƽ��ʱCO2��ת����Ϊ50%�����������ƽ�ⳣ��K1=
��2���ڣ�1���Ļ����ϣ�����ϵ�¶Ƚ���800�森��֪�������µ�ƽ�ⳣ��K2=0.81��������֪�÷�Ӧ������ӦΪ
��3���ڣ�1���Ļ����ϣ�ѹ���������֮0.5L���������µ�ƽ�ⳣ��ΪK3����K3
��4��830��ʱ��ijʱ�̲����ϵ�и����ʵ������£�n��CO2��=1.2mol��n��H2��=1.5mol��
n��CO��=0.9mol��n��H2O��=0.9mol�����ʱ�÷�Ӧ
���������Ӧ�������淴Ӧ������ƽ��״̬������
���㣺�û�ѧƽ�ⳣ�����м���
ר�⣺
��������1����������ʽ����ƽ��ʱ����ֵ�ƽ��Ũ�ȣ�����ƽ�ⳣ������ʽ���㣻
��2�����ݻ�ѧƽ������ʽ��ʽ����ƽ��Ũ�ȣ����ƽ�ⳣ���������õ���Ӧ��ƽ�ⳣ������800��Cƽ�ⳣ���Ƚ��ж������仯��
��3��ƽ�ⳣ�����¶ȵĺ�����
��4������Ũ���̼����ƽ�ⳣ���ȽϷ����жϷ�Ӧ���еķ���
��2�����ݻ�ѧƽ������ʽ��ʽ����ƽ��Ũ�ȣ����ƽ�ⳣ���������õ���Ӧ��ƽ�ⳣ������800��Cƽ�ⳣ���Ƚ��ж������仯��
��3��ƽ�ⳣ�����¶ȵĺ�����
��4������Ũ���̼����ƽ�ⳣ���ȽϷ����жϷ�Ӧ���еķ���
���
�⣺��1����Ӧ�ﵽƽ��ʱCO2��ת����Ϊ50%��ƽ��ʱCO2��Ũ��Ϊ1mol/L����
CO2��g��+H2��g��?CO��g��+H2O��g��
��ʼ��mol/L����2 2 0 0
�仯��mol/L����1 1 1 1
��ʼ��mol/L����1 1 1 1
��830��÷�Ӧ��ƽ�ⳣ��k=
=1���ʴ�Ϊ��1��
��2��������ϵ�¶Ƚ���800�����ƽ�ⳣ��K1=0.81��K=1��˵�������¶�ƽ�ⳣ����С��ƽ��������У�����Ϊ���ȷ�Ӧ������ӦΪ���ȷ�Ӧ���ʴ�Ϊ�����ȣ�
��3��ƽ�ⳣ�����¶ȵĺ������¶Ȳ��䣬ƽ�ⳣ�����䣬�ʴ�Ϊ��=��
��4��T��ʱ��ijʱ�̲����ϵ�и����ʵ������£�n��CO2��=1.2mol��n��H2��=1.5mol��n��CO��=0.9mol��n��H2O��=0.9mol��Q=
=0.45��С��ƽ�ⳣ������Ӧ������У��ʴ�Ϊ��������Ӧ����
CO2��g��+H2��g��?CO��g��+H2O��g��
��ʼ��mol/L����2 2 0 0
�仯��mol/L����1 1 1 1
��ʼ��mol/L����1 1 1 1
��830��÷�Ӧ��ƽ�ⳣ��k=
| 1��1 |
| 1��1 |
��2��������ϵ�¶Ƚ���800�����ƽ�ⳣ��K1=0.81��K=1��˵�������¶�ƽ�ⳣ����С��ƽ��������У�����Ϊ���ȷ�Ӧ������ӦΪ���ȷ�Ӧ���ʴ�Ϊ�����ȣ�
��3��ƽ�ⳣ�����¶ȵĺ������¶Ȳ��䣬ƽ�ⳣ�����䣬�ʴ�Ϊ��=��
��4��T��ʱ��ijʱ�̲����ϵ�и����ʵ������£�n��CO2��=1.2mol��n��H2��=1.5mol��n��CO��=0.9mol��n��H2O��=0.9mol��Q=
| 0.9��0.9 |
| 1.2��1.5 |
���������⿼�黯ѧƽ���Լ���Ӧ���ʵ����⣬ƽ�ⳣ��������жϣ���Ŀ�Ѷ��еȣ�ע��ͼ�����߱仯�ķ�����������������Է�Ӧ���ʺ�ƽ���ƶ���Ӱ�죮

��ϰ��ϵ�д�
�����Ŀ
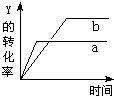 ��Ӧ X������+Y������?2Z������+Q��Q��0������һ�������£���Ӧ��Y��ת�����뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ����ʹ����a��Ϊ����b�ɲ�ȡ�Ĵ�ʩ�ǣ�������
��Ӧ X������+Y������?2Z������+Q��Q��0������һ�������£���Ӧ��Y��ת�����뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ����ʹ����a��Ϊ����b�ɲ�ȡ�Ĵ�ʩ�ǣ�������| A��������� | B�������¶� |
| C������ѹǿ | D������Y��Ũ�� |
���й��ڸ�˹���ɵ�˵������ȷ���ǣ�������
| A�����ܷ�Ӧ��һ����ɻ��Ƿּ�����ɣ��䷴Ӧ����ͬ |
| B����Ӧ��ֻ�뷴Ӧ��ϵ��ʼ̬����̬�йأ����뷴Ӧ��;���� |
| C�����ݸ�˹���ɣ��Ȼ�ѧ����ʽ�С�Hֱ����Ӽ��ɵ��ܷ�Ӧ�� |
| D����Щ��Ӧ�ķ�Ӧ�Ȳ���ֱ�Ӳ�ã���ͨ����˹���ɼ�Ӽ���õ� |
����˵����ȷ���ǣ�������
| A���������ڴ����ң���Ԫ���γɵļ����Ӱ뾶��С |
| B�����ۻ�������һ�������Թ��ۼ������ܺ��Ǽ��Թ��ۼ� |
| C����VIIA��Ԫ�ش��ϵ��£�����̬�⻯����ȶ��Ժͻ�ԭ�Ծ�����ǿ |
| D�����ܴ��ڻ�̬��������Ų�ʽΪ1s22s22p63s23p64s24p5��ԭ�� |
ij��Һ�д��ڴ�����K+��OH-��CO32-������Һ�л����ܴ������ڵ��ǣ�������
| A��NH4+ |
| B��Ca2+ |
| C��HCO3- |
| D��SO42- |
Ag2O2����п���Ե�ص������������ʣ��������ҺΪKOH ��Һ����طŵ�ʱ�ܷ�Ӧ����ʽΪ��Ag2O2+2Zn+4KOH+2H2O=2K2Zn��OH��4+2Ag�������йظõ�ص�˵����ȷ���ǣ�������
| A���ŵ�ʱ��������Һ��pH��� |
| B��K2Zn��OH��4�ǻ�ԭ���Ag���������� |
| C��ÿ����1 mol K2Zn��OH��4 ת�� 2 mol ���� |
| D���õ��������ӦʽΪ��Ag2O2+2 e-+2H2O=2Ag+4OH- |
 һ���¶��£����ݻ�Ϊ2L���ܱ�������ͨ���������巢����ѧ��Ӧ����Ӧ�и����ʵ����ʵ����仯��ͼ��ʾ����ش��������⣺
һ���¶��£����ݻ�Ϊ2L���ܱ�������ͨ���������巢����ѧ��Ӧ����Ӧ�и����ʵ����ʵ����仯��ͼ��ʾ����ش��������⣺