题目内容
9.下列离子方程式书写正确的是( )| A. | FeCl2溶液中通入Cl2:Fe2++Cl2═Fe3++2Cl- | |
| B. | Mg(OH)2与盐酸的反应:OH-+H+═H2O | |
| C. | Al(OH)3沉淀中滴加盐酸:Al(OH)3+3H+═Al3++3H2O | |
| D. | AlCl3溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O |
分析 A.电子、电荷不守恒;
B.氢氧化镁在离子反应中保留化学式;
C.反应生成氯化铝和水;
D.一水合氨在离子反应中保留化学式.
解答 解:A.FeCl2溶液中通入Cl2的离子反应为2Fe2++Cl2═2Fe3++2Cl-,故A错误;
B.Mg(OH)2与盐酸的反应的离子反应为Mg(OH)2+2H+═2H2O+Mg2+,故B错误;
C.Al(OH)3沉淀中滴加盐酸的离子反应为Al(OH)3+3H+═Al3++3H2O,故C正确;
D.AlCl3溶液中加入过量氨水的离子反应为Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故D错误;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
2.现有20gD2O和36gH2O,下列说法不正确的是( )
| A. | 它们的分子数之比为1:2 | |
| B. | 它们的中子数之比为5:8 | |
| C. | 它们的电子数之比为1:2 | |
| D. | 分别与1mol钠反应,生成气体的质量比为1:1 |
20.在由水电离出的c(H+)水•c(OH-)水=10-24的溶液中一定大量共存的离子组是( )
| A. | Fe2+、Na+、NO3-、Cl- | B. | Ba2+、Na+、NO3-、Cl- | ||
| C. | SO42-、SO32-、NH4+、Na+ | D. | Mg2+、Na+、Br-、AlO2- |
17.含有0.20mol碳酸钠的溶液250mL和100mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
| A. | 2.0mol/L | B. | 0.24mol/L | C. | 0.19 mol/L | D. | 3 mol/L |
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2 L 水中含有的分子数为0.5NA | |
| B. | 标准状况下,22.4LN2中含有的原子数为NA | |
| C. | 23g Na与足量H2O反应转移的电子数为NA | |
| D. | 物质的量浓度为1 mol•Lˉ1的K2SO4溶液中,含2 NA个K+ |
14.已知:2CO(g)+O2(g)═2CO2(g);△H=-566kJ/mol
Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}{{O}_2}({g})$;△H=-226kJ/mol
根据以上热化学方程式判断,下列说法不正确的是( )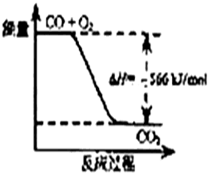
Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}{{O}_2}({g})$;△H=-226kJ/mol
根据以上热化学方程式判断,下列说法不正确的是( )

| A. | CO的燃烧热为283 kJ/mol | |
| B. | 图可表示由CO生成CO2的反应过程和能量关系 | |
| C. | 2Na2O2(s)+2CO2(s)═2Na2CO3(s)+O2(g)△H>-452 kJ/mol | |
| D. | CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为1.204×1024 |
18.下列实验操作中,正确的是( )
| A. |  称量 | B. | 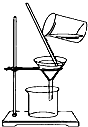 转移 | ||
| C. | 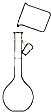 过滤 | D. |  蒸馏 |