题目内容
3.某化合物通过化合反应生成,向其水溶液中加入足量Na2O2,最终有白色沉淀产生.下列化合物中符合上述条件的是( )| A. | Ca(HCO3)2 | B. | Na2S | C. | FeI2 | D. | AlCl3 |
分析 两种或者多种物质反应生成一种物质的反应为化合反应,过氧化钠先和水反应生成氢氧化钠和氧气,氢氧化钠再和盐反应,根据生成物判断反应现象.
解答 解:A.Ca(HCO3)2可由碳酸钙与二氧化碳、水化合生成,过氧化钠先和水反应生成氢氧化钠和氧气,氢氧化钠和Ca(HCO3)2反应,生成白色碳酸钙沉淀,故A正确;
B.硫化钠可以硫与钠化合得到,硫化钠溶液中加入过氧化钠,过氧化钠能氧化硫离子生成单质硫,单质硫为淡黄色沉淀,故B错误;
C.铁与碘化合生生成碘化亚铁,碘化亚铁溶液中加入过氧化钠,氧化碘离子生成单质碘,碘溶液水生成碘的水溶液,得不到沉淀,故C错误;
D.氯化铝可由铝与氯气化合反应生成,过氧化钠先和水反应生成氢氧化钠和氧气,过量的氢氧化钠和氯化铝反应生成偏铝酸钠,故D错误;
故选:A.
点评 本题考查了过氧化钠和水、盐溶液反应的现象,熟悉过氧化钠的氧化性,明确过氧化钠与溶液反应实质是解题关键,难度不大,注意根据反应生成物判断反应现象,从而确定选项.

练习册系列答案
 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
13.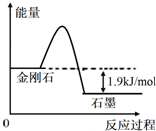 根据表中的信息判断下列说法错误的是( )
根据表中的信息判断下列说法错误的是( )
 根据表中的信息判断下列说法错误的是( )
根据表中的信息判断下列说法错误的是( )| 物质 | 总键能/(kJ•mol-1) | 燃烧热/(kJ•mol-1) |
| 金刚石 | a | 395.4 |
| 石墨 | b | 393.5 |
| A. | 由表中信息可得如右图所示的图象 | |
| B. | 由表中信息知C(石墨,s)=C(金刚石,s)△H=+1.9kJ/mol | |
| C. | 由表中信息可推知a<b | |
| D. | 表示石墨燃烧热的热化学方程式为C(石墨,s)+1/2O2(g)═CO(g)△H=-393.5kJ/mol |
14.某学生的实验报告所列出的下列数据中合理的是( )
| A. | 用10 mL量筒量取7.13 mL盐酸 | |
| B. | 用广泛pH试纸测得某溶液的pH为2.3 | |
| C. | 用25ml酸式滴定管量取21.70 mLKMnO4溶液 | |
| D. | 用托盘天平称量25.20 g NaCl |
11.一定条件下在2L的密闭容器中,充入2mol SO2和1molO2发生反应:
2SO2(g)+O2(g)?2SO3(g)△H=-196kJ•moL-1,当气体的总物质的量减少0.8mol时反应达到平衡,下列有关叙述不正确的是( )
2SO2(g)+O2(g)?2SO3(g)△H=-196kJ•moL-1,当气体的总物质的量减少0.8mol时反应达到平衡,下列有关叙述不正确的是( )
| A. | 保持温度不变,向平衡后的容器中再充入1molSO2和0.5molO2时,V(正)>V(逆) | |
| B. | 相同温度下,起始时向容器中充入2mol SO3,达平衡时SO3的转化率为20% | |
| C. | 平衡混合气体中SO2的物质的量为1.2mol | |
| D. | 保持其他条件不变,若起始时向容器中充入2molSO3,达平衡时吸收39.2kJ的热量 |
18.短周期主族元素X、Y、Z在元素周期表中的相对位置如图所示.下列说法一定正确的是( )
| X | Y |
| Z |
| A. | 气态氢化物的沸点:X<Y<Z | |
| B. | 最高正化合价:Y>X | |
| C. | X、Y、Z的最高价氧化物对应水化物中,Z的酸性最强 | |
| D. | 若X、Y、Z的原子序数之和等于25,则它们都是非金属元素 |
15.我国发生的“三聚氰胺奶制品事件”已经造成多名患儿死亡.三聚氰胺是由碳、氢、氧、氮等元素组成,不法分子在奶制品中添加三聚氰胺的目的是为了提高牛奶中下列哪种成分的含量( )
| A. | 油脂 | B. | 矿物质 | C. | 蛋白质 | D. | 维生素 |
12.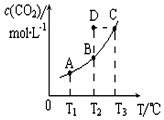 恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法错误的是( )
恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法错误的是( )
 恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法错误的是( )
恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法错误的是( )| A. | 在T2时,若反应进行到状态D,则一定有v正<v逆 | |
| B. | 平衡状态A与C相比,平衡状态A的c(CO)小 | |
| C. | 若T1、T2时的平衡常数分别为K1、K2,则K1<K2 | |
| D. | 反应CO(g)+H2O(g)?CO2(g)+H2(g)的△H>0 |
6.甲醇汽油是由10%~25%的甲醇与其他化工原料、添加剂合成的新型车用燃料,可达到国标汽油的性能和指标.工业上合成甲醇一般采用下列反应:CO(g)+2H2(g)?CH3OH(g)△H=a kJ/mol,
下表是该反应在不同温度下的化学平衡常数(K):
(1)由表中数据判断,反应中a<0(填“>”、“=”或“<”).
(2)某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5mol•L-1,则此时的温度为310℃.
(3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
①反应从2 min到4min之间,H2的反应速率为0.3mol/(L•min).
②反应达到平衡时CO的转化率为62.5%.
③反应在第2min时改变了反应条件,改变的条件可能是A(填序号).
A.使用催化剂 B.降低温度 C.增加H2的浓度
(4)向容积相同、温度分别为T1和T2的两个密闭容器中均充入1 molCO和2mol H2,发生反应CO(g)+2 H2(g)?CH3OH(g)△H=a kJ/mol.恒温恒容下反应相同时间后,分别测得体系中CO的百分含量分别为w1和w2;
已知T1<T2,则ω1Dω2(填序号).
A.大于 B.小于 C.等于 D.以上都有可能.
下表是该反应在不同温度下的化学平衡常数(K):
| 温度/℃ | 250 | 310 | 350 |
| K | 2.041 | 0.250 | 0.012 |
(2)某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5mol•L-1,则此时的温度为310℃.
(3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
| 时间/min/浓度mol/L | c(CO) | c(H2) | c(CH3OH) |
| 0 | 0.8 | 1.6 | 0 |
| 2 | 0.6 | 1.2 | 0.2 |
| 4 | 0.3 | 0.6 | 0.5 |
| 6 | 0.3 | 0.6 | 0.5 |
②反应达到平衡时CO的转化率为62.5%.
③反应在第2min时改变了反应条件,改变的条件可能是A(填序号).
A.使用催化剂 B.降低温度 C.增加H2的浓度
(4)向容积相同、温度分别为T1和T2的两个密闭容器中均充入1 molCO和2mol H2,发生反应CO(g)+2 H2(g)?CH3OH(g)△H=a kJ/mol.恒温恒容下反应相同时间后,分别测得体系中CO的百分含量分别为w1和w2;
已知T1<T2,则ω1Dω2(填序号).
A.大于 B.小于 C.等于 D.以上都有可能.