题目内容
在一定温度下,在一体积固定的密闭容器中加入2 mol X和1 mol Y,发生如下反应:2X(g)+Y(g)![]() aZ(g)+W(g) ΔH=-Q kJ·mol-1 (Q>0)
aZ(g)+W(g) ΔH=-Q kJ·mol-1 (Q>0)
当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;平衡后再升高温度,混合气体的平均相对分子质量减小,则
(1)温度升高,平衡常数K的值是______________(填“增大”“减小”或“不变”)。
(2)化学计量数a的值为______________。
(3)有同学认为,Q1一定小于Q,你认为该结论是否正确?______________,其理由是_____
_____________________________________________________________________。
(4)维持温度不变,若起始时向容器中加入的物质的量如下列各项,则反应达到平衡后放出的热量仍为Q1 kJ的是______________ (稀有气体不参与反应)。
A.2 mol X、1 mol Y、1 mol Ar
B.a mol Z、1 mol W
C.1 mol X、0.5 mol Y、
D.2 mol X、1 mol Y、1 mol Z
(5)X的转化率α=______________(用含Q、Q1的代数式表示)。
(1)减小
(2)1
(3)正确 2 mol X和1 mol Y不可能完全反应
(4)A
(5)![]() ×100%
×100%
解析:平衡后升高温度,平衡向逆反应方向移动,混合气体的平均相对分子质量减小,故a<2,所以a=1,温度升高,平衡常数K值减小。
2 mol X和1 mol Y不可能完全反应,所以放出的热量Q1<Q。
反应放出的热量与2 mol X和1 mol Y达到平衡时一样,必须充入时完全一致,A项中加入Ar对平衡无影响,故为A。
(5)X的转化率为![]() ×100%。
×100%。


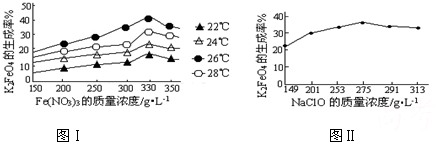
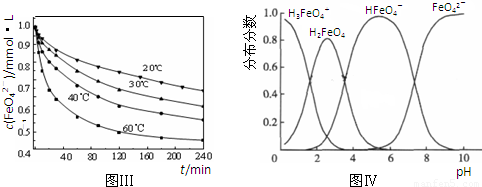
 4Fe(OH)3+8OH-+3O2↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
4Fe(OH)3+8OH-+3O2↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
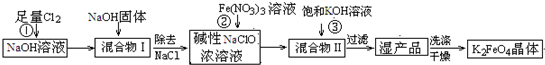


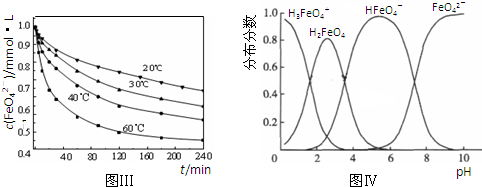
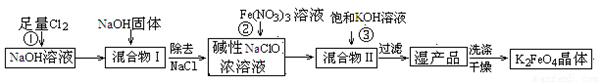
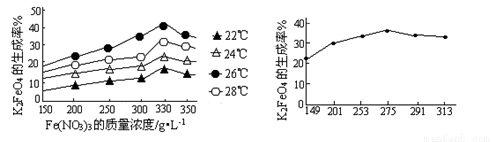
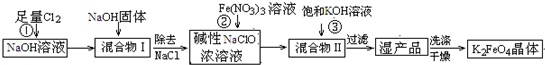
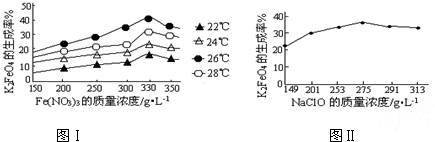
 4Fe(OH)3+8OH-+3O2↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用______溶液(填序号).
4Fe(OH)3+8OH-+3O2↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用______溶液(填序号).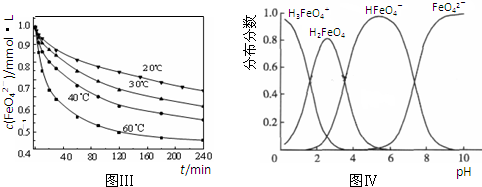
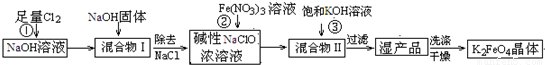
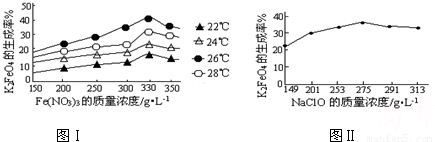
 4Fe(OH)3+8OH-+3O2↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用______溶液(填序号).
4Fe(OH)3+8OH-+3O2↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用______溶液(填序号).