题目内容
6.将a气体通入b溶液中,实验现象描述正确的组合是| a气体 | b溶液 | 预测的现象 | |
| ① | C02 | BaCl2溶液 | 白色沉淀析出 |
| ② | SO2 | Ba(NO3)2 溶液 | 白色沉淀析出 |
| ③ | Br2 | AgNO3溶液 | 淡黄色沉淀析出 |
| ④ | NH3 | AlCl3溶液 | 白色沉淀析出 |
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①③④ |
分析 ①氯化钡溶液不与二氧化碳反应;
②SO2通入水中生成H2SO3,溶液呈酸性,NO3-在酸性条件下具有强氧化性,可与H2SO3发生氧化还原反应生成SO42-;
③Br2通入水中和水反应生成氢溴酸和次溴酸,溴离子和银离子反应生成溴化银沉淀;
④氨气溶于水生成一水合氨,一水合氨和氯化铝反应生成白色的氢氧化铝沉淀.
解答 解:①二氧化碳和氯化钡溶液不发生反应,则不会出现白色沉淀,故①错误;
②SO2通入水中生成H2SO3,溶液呈酸性,NO3-在酸性条件下具有强氧化性,可发生反应:3SO2+2H2O+2NO3-+3Ba2+=3BaSO4↓+4H++2NO↑,会出现白色沉淀析出,故②正确;
③Br2通入水中和水反应生成氢溴酸和次溴酸,溴离子和银离子反应生成溴化银沉淀,则会析出淡黄色沉淀,故③正确;
④氨水是弱碱,不能溶解氢氧化铝,氯化铝溶液加入过量氨水的反应方程式为:AlCl3+3NH3•H2O═Al(OH)3↓+3NH4Cl,会出现白色沉淀析出,故④正确;
故选B.
点评 本题主要考查了参加气体的性质及检验方法,题目难度中等,明确常见气体的性质为解答关键,注意NO3-在酸性条件下具有强氧化性,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
16.室温下,将0.4mol/L一元酸HA溶液和0.2mol/LNaOH溶液等体积混合(忽略混合时溶液体积的变化),测得混合液的pH=5,则下列说法或粒子浓度关系式正确的是( )
| A. | 混合液中由水电离出的c(H+)=1×10-8mol/L | |
| B. | c(A-)+c(HA)=2c(Na+)=0.4mol/L | |
| C. | HA溶液中$\frac{c({A}^{-})}{c(HA)•c(O{H}^{-})}$与混合液中$\frac{c({A}^{-})}{c(HA)•c(O{H}^{-})}$相等 | |
| D. | c(A-)-c(HA)=2c(OH-)-2c(H+) |
17.化学与工农业生产和人类生活密切相关.下列说法中正确的是( )
| A. | 酸雨就是pH<7的雨水,主要是由大气中的SO2、NO2等造成的 | |
| B. | 饱和氯水既有酸性又有漂白性,加入NaHCO₃后漂白性减弱 | |
| C. | 烧融烧碱应选用的器皿是铁坩埚而不是石英坩埚、普通玻璃坩埚或陶瓷坩埚 | |
| D. | 用纯碱制玻璃、用铁矿石炼铁、用氨制碳酸铵都会产生温室气体 |
14.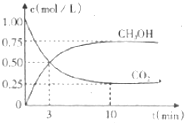 固定和利用C02.能存效地利用资源,并减少空气中的温室气体.工业上正在研究利用C02来生产甲醇燃料的方法,该方法的化学方程式是C02 (g)+3H2 (g)?CH30H (g)+H2O(g)△H=-49.0kJ/mol,在体积为1L的密闭容器中,充人1molCO2和4molH2,一定条件下发生反应:测得C02和CH30H(g)的浓度随时间变化如图所示.下列说法正确的是
固定和利用C02.能存效地利用资源,并减少空气中的温室气体.工业上正在研究利用C02来生产甲醇燃料的方法,该方法的化学方程式是C02 (g)+3H2 (g)?CH30H (g)+H2O(g)△H=-49.0kJ/mol,在体积为1L的密闭容器中,充人1molCO2和4molH2,一定条件下发生反应:测得C02和CH30H(g)的浓度随时间变化如图所示.下列说法正确的是
( )
 固定和利用C02.能存效地利用资源,并减少空气中的温室气体.工业上正在研究利用C02来生产甲醇燃料的方法,该方法的化学方程式是C02 (g)+3H2 (g)?CH30H (g)+H2O(g)△H=-49.0kJ/mol,在体积为1L的密闭容器中,充人1molCO2和4molH2,一定条件下发生反应:测得C02和CH30H(g)的浓度随时间变化如图所示.下列说法正确的是
固定和利用C02.能存效地利用资源,并减少空气中的温室气体.工业上正在研究利用C02来生产甲醇燃料的方法,该方法的化学方程式是C02 (g)+3H2 (g)?CH30H (g)+H2O(g)△H=-49.0kJ/mol,在体积为1L的密闭容器中,充人1molCO2和4molH2,一定条件下发生反应:测得C02和CH30H(g)的浓度随时间变化如图所示.下列说法正确的是( )
| A. | 该反应在高温条件下能向发进行 | |
| B. | 充人 He(g).能使 $\frac{n(C{H}_{3}OH)}{n(C{0}_{2})}$增大 | |
| C. | 再充入1molCO2和4molH2,能使$\frac{n(C{H}_{2}OH)}{n(C{O}_{2})}$增大 | |
| D. | 容器内气体密度不再改变说明该飞应达到平衡状态 |
1.科学家在研究化学物质吋,常常对物质逬行分类,以便对同类物质的组成和性质进行深人的研究,下列4组物质:
①Ca、S、Cl2、NO2②NH3•H2O、Na2CO3、CH4、KCl③H2CO3、H2SO4、NaOH、H2SiO3④MgO、SO2、CO2、SiO2从物质的基本分类看,每组中都有一种物质与其它物质不属于同这4种物质分别是( )
①Ca、S、Cl2、NO2②NH3•H2O、Na2CO3、CH4、KCl③H2CO3、H2SO4、NaOH、H2SiO3④MgO、SO2、CO2、SiO2从物质的基本分类看,每组中都有一种物质与其它物质不属于同这4种物质分别是( )
| A. | NO2、CH4、NaOH、MgO | B. | Cl2、NH3•H20、NaOH、Si02 | ||
| C. | Ca、Ma2C03、H2Si03、MgO | D. | NO2、CH4、H2SiO3、SO2 |
18.常温下,下列试剂不能用带玻璃塞的试剂瓶盛放的是( )
| A. | 浓盐酸 | B. | 浓硝酸 | C. | 稀盐酸 | D. | 氢氧化钠溶液 |
15.T℃时,A气体与B气体反应生成C气体.反应过程中A、B、C浓度变化如图(1)所示,若保持其他条件不变,温度分别为T1℃和T2℃时,B的体积分数与时间的关系如图(2)所示,则下列结论正确的是( )
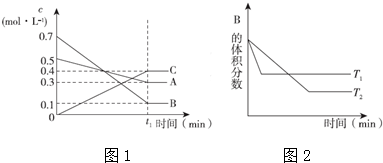

| A. | 该平衡体系的化学反应方程式为:3A(g)+B(g)═4 C(g) | |
| B. | 在t1时间内用B表示该反应的平均速率为0.6/t1mol•L-1•min-1 | |
| C. | 其他条件不变,升高温度,正反应速率减小、逆反应速率增大,A的转化率减小 | |
| D. | 维持温度和容器体积不变,往平衡体系中充惰性气体,C的百分含量增大 |
16.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 22.4L氯气与足量的钠反应,转移的电子数为2NA | |
| B. | 常温常压下,32gO3或O2中含有的氧原子数都为2NA | |
| C. | 1 mol氯气与足量水反应时,转移的电子数为2NA | |
| D. | 含2 mol H2SO4的浓硫酸与足量铜反应,转移的电子数为2NA |
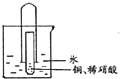 为了探究一氧化氮、二氧化氮、硝酸之间的相互转化,有同学设计了如下实验:如图将少量铜片装入小试管中,再加人适量稀硝酸,然后迅速将大试管倒扣在小试管外.将套好的大、小试管一起竖立在烧杯中,使水浸没大试管口.充分反应完后,通过弯玻璃管往大试管中吹人足量空气,并往烧杯中滴人几滴紫色石蕊试液.试回答:
为了探究一氧化氮、二氧化氮、硝酸之间的相互转化,有同学设计了如下实验:如图将少量铜片装入小试管中,再加人适量稀硝酸,然后迅速将大试管倒扣在小试管外.将套好的大、小试管一起竖立在烧杯中,使水浸没大试管口.充分反应完后,通过弯玻璃管往大试管中吹人足量空气,并往烧杯中滴人几滴紫色石蕊试液.试回答: