题目内容
下列离子方程式与所述事实相符且正确的是( )
| A、向NaClO溶液中通入少量二氧化硫 3ClO-+SO2+H2O═2HClO+SO42-+Cl- |
| B、碳酸氢钙与过量的NaOH溶液反应Ca2++HCO3-+OH-═CaCO3↓+H2O |
| C、用二氧化硫水溶液吸收溴蒸气:SO2+Br2+2H2O═SO42-+2H++2HBr |
| D、在碳酸氢铵稀溶液中加入足量的氢氧化钠稀溶液:NH4++OH-═NH3?H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.次氯酸根离子具有氧化性能够氧化二氧化硫;
B.碳酸氢钙与过量的NaOH溶液反应生成碳酸钙和碳酸钠、水;
C.氢溴酸为强电解质应拆成离子;
D.漏掉碳酸氢根离子与氢氧根离子的反应.
B.碳酸氢钙与过量的NaOH溶液反应生成碳酸钙和碳酸钠、水;
C.氢溴酸为强电解质应拆成离子;
D.漏掉碳酸氢根离子与氢氧根离子的反应.
解答:
解:A.向NaClO溶液中通入少量二氧化硫,离子方程式为:3ClO-+SO2+H2O═2HClO+SO42-+Cl-,故A正确;
B.碳酸氢钙与过量的NaOH溶液反应Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-,故B错误;
C.用二氧化硫水溶液吸收溴蒸气,离子方程式:SO2+Br2+2H2O═SO42-+4H++Br-,故C错误;
D.在碳酸氢铵稀溶液中加入足量的氢氧化钠稀溶液,离子方程式:NH4++HCO3-+2OH-═NH3?H2O+H2O+CO32-,故D错误;
故选:A.
B.碳酸氢钙与过量的NaOH溶液反应Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-,故B错误;
C.用二氧化硫水溶液吸收溴蒸气,离子方程式:SO2+Br2+2H2O═SO42-+4H++Br-,故C错误;
D.在碳酸氢铵稀溶液中加入足量的氢氧化钠稀溶液,离子方程式:NH4++HCO3-+2OH-═NH3?H2O+H2O+CO32-,故D错误;
故选:A.
点评:本题考查了离子方程式的书写,题目难度不大,明确反应的实质是解题关键,注意反应物用量多少对反应的影响.

练习册系列答案
相关题目
下列化学用语表达正确的是( )
A、丙烷分子的球棍模型: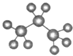 |
B、Na2S的电子式: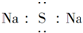 |
| C、乙烯的结构简式:CH2CH2 |
| D、氯仿的化学式:CCl4 |
下列离子方程式正确的是( )
A、硫酸镁溶液跟氢氧化钡溶液反应:S
| ||
| B、硫酸和氢氧化铜溶液混合:H++OH-=H2O | ||
| C、铜片插入硝酸银溶液中:Cu+2Ag+═Cu2++2Ag | ||
| D、澄清石灰水中加入盐酸:Ca(OH)2+2H+=Ca2++2H2O |
下列有关化学概念或原理的论述中,正确的是( )
| A、任何一个氧化还原反应都可以设计为电池,输出电能 |
| B、铅蓄电池放电时的负极和充电时的阴极均发生氧化反应 |
| C、电解饱和食盐水的过程中,水的电离平衡正向移动 |
| D、任何可逆反应,其平衡常数越大,反应速率、反应物的转化率就越大 |
设NA代表阿伏加德罗常数的值,下列说法中不正确的是( )
| A、7.8g过氧化钠与足量二氧化碳反应转移的电子数为0.1NA |
| B、8.4gNaHCO3固体中含HCO3-数目为0.1NA |
| C、1mol氯气与氢氧化钙完全反应生成氯化钙和次氯酸钙,转移的电子数为2NA |
| D、常温下,4.6gNa和足量的O2完全反应失去电子数为0.2NA |
在标准状况下,某烧瓶内装满HCl气体,将此烧瓶倒扣在盛水的水槽内,当液面上升到烧瓶容积的
时,此时烧瓶内溶液的物质的量浓度是( )
| 3 |
| 5 |
| A、0.74mol/L |
| B、0.045mol/L |
| C、0.037mol/L |
| D、0.025mol/L |
分子中有3个-CH3的C5H12,其可能的结构有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
 如图为原电池装置示意图,
如图为原电池装置示意图,