题目内容
Ⅰ.通常状况下,X、Y和Z是三种气态单质.X的组成元素是第三周期原子半径最小的元素(稀有气体元素除外);Y和Z均由元素R组成,反应Y+2I-+2H+═I2+Z+H2O常作为Y的鉴定反应.W是短周期元素,最外层电子数是最内层电子数的三倍,吸引电子对的能力比X单质的组成元素要弱.
(1)Z的化学式 .
(2)将Y和二氧化硫分别通入品红溶液,都能使品红褪色.简述用褪色的溶液区别Y和二氧化硫的实验方法: .
(3)举出实例说明X的氧化性比W单质氧化性强(仅用一个化学方程式表示): .
Ⅱ.如图1是0.1mol?L-1四种电解质溶液的pH随温度变化的图象.
(1)其中符合0.1mol?L-1 NH4Al(SO4)2的pH随温度变化的曲线是 (填写序号),
(2)20℃时,0.1mol?L-1 NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)= .(计算精确值)
(3)室温时,向100mL 0.1mol?L-1 NH4HSO4溶液中滴加0.1mol?L-1 NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图2:

试分析图中a、b、c、d四个点,水的电离程度最大是 点;在b点,溶液中各离子浓度由大到小的排列顺序是 .
(1)Z的化学式
(2)将Y和二氧化硫分别通入品红溶液,都能使品红褪色.简述用褪色的溶液区别Y和二氧化硫的实验方法:
(3)举出实例说明X的氧化性比W单质氧化性强(仅用一个化学方程式表示):
Ⅱ.如图1是0.1mol?L-1四种电解质溶液的pH随温度变化的图象.
(1)其中符合0.1mol?L-1 NH4Al(SO4)2的pH随温度变化的曲线是
(2)20℃时,0.1mol?L-1 NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=
(3)室温时,向100mL 0.1mol?L-1 NH4HSO4溶液中滴加0.1mol?L-1 NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图2:

试分析图中a、b、c、d四个点,水的电离程度最大是
考点:位置结构性质的相互关系应用,弱电解质在水溶液中的电离平衡
专题:元素周期律与元素周期表专题,电离平衡与溶液的pH专题
分析:Ⅰ.通常状况下,X、Y和Z是三种气态单质.X的组成元素是第三周期原子半径最小的元素(稀有气体元素除外),则X为Cl2;Y和Z均由元素R组成,反应Y+2I-+2H+═I2+Z+H2O常作为Y的鉴定反应,由元素守恒可知,Y、Z为O元素的同素异形体,R为O元素;可推知Y为O3、Z为O2;W是短周期元素,最外层电子数是最内层电子数的三倍,最外层电子数为6,则W为S元素;
Ⅱ.(1)NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大;
(2)根据电荷守恒进行解答;
(3)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3?H2O,(NH4)2SO4可以促进水的电离,而NH3?H2O抑制水的电离,b点溶液呈中性,据此解答.
Ⅱ.(1)NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大;
(2)根据电荷守恒进行解答;
(3)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3?H2O,(NH4)2SO4可以促进水的电离,而NH3?H2O抑制水的电离,b点溶液呈中性,据此解答.
解答:
解:Ⅰ.通常状况下,X、Y和Z是三种气态单质.X的组成元素是第三周期原子半径最小的元素(稀有气体元素除外),则X为Cl2;Y和Z均由元素R组成,反应Y+2I-+2H+═I2+Z+H2O常作为Y的鉴定反应,由元素守恒可知,Y、Z为O元素的同素异形体,R为O元素;可推知Y为O3、Z为O2;W是短周期元素,最外层电子数是最内层电子数的三倍,最外层电子数为6,则W为S元素,则:
(1)由上述分析可知,Z的化学式为O2,故答案为:O2;
(2)将O3和二氧化硫分别通入品红溶液,都能使品红褪色.简述用褪色的溶液区别O3和二氧化硫的实验方法为:加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO2;若溶液不变红,则原通入气体是O3,
故答案为:加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO2;若溶液不变红,则原通入气体是O3;
(3)说明Cl2的氧化性比D单质氧化性强的化学方程式为:H2S+Cl2═S+2HCl,
故答案为:H2S+Cl2═S+2HCl;
Ⅱ.(1)NH4Al(SO4)2为强酸弱碱盐,其溶液呈酸性,升高温度促进水解,导致溶液酸性增强,溶液的pH减小,
故答案为:I;
(2)根据电荷守恒得2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3 mol?L-1-10-11mol?L-1=(10-3-10-11)mol?L-1,
故答案为:(10-3-10-11)mol?L-1;
(3)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3?H2O,(NH4)2SO4可以促进水的电离,而NH3?H2O抑制水的电离,b点溶液呈中性,故a点水的电离程度最大,
b点溶液含有(NH4)2SO4、Na2SO4、NH3?H2O三种成分,a点时溶液中(NH4)2SO4与Na2SO4各是0.05mol、0.05mol,a点时c(Na+)=c(SO42-),故b点时c(Na+)>c(SO42-),根据N元素与S元素的关系,可以得出c(SO42-)>c(NH4+),故c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+),
故答案为:a;c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
(1)由上述分析可知,Z的化学式为O2,故答案为:O2;
(2)将O3和二氧化硫分别通入品红溶液,都能使品红褪色.简述用褪色的溶液区别O3和二氧化硫的实验方法为:加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO2;若溶液不变红,则原通入气体是O3,
故答案为:加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO2;若溶液不变红,则原通入气体是O3;
(3)说明Cl2的氧化性比D单质氧化性强的化学方程式为:H2S+Cl2═S+2HCl,
故答案为:H2S+Cl2═S+2HCl;
Ⅱ.(1)NH4Al(SO4)2为强酸弱碱盐,其溶液呈酸性,升高温度促进水解,导致溶液酸性增强,溶液的pH减小,
故答案为:I;
(2)根据电荷守恒得2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3 mol?L-1-10-11mol?L-1=(10-3-10-11)mol?L-1,
故答案为:(10-3-10-11)mol?L-1;
(3)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3?H2O,(NH4)2SO4可以促进水的电离,而NH3?H2O抑制水的电离,b点溶液呈中性,故a点水的电离程度最大,
b点溶液含有(NH4)2SO4、Na2SO4、NH3?H2O三种成分,a点时溶液中(NH4)2SO4与Na2SO4各是0.05mol、0.05mol,a点时c(Na+)=c(SO42-),故b点时c(Na+)>c(SO42-),根据N元素与S元素的关系,可以得出c(SO42-)>c(NH4+),故c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+),
故答案为:a;c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
点评:本题属于拼合型题目,涉及元素化合物推断、盐类水解、离子浓度大小比较等知识点,Ⅱ(3)是难点,知道图象中各个点的溶质即可解答,注意确定离子浓度大小时要结合电荷守恒、物料守恒来分析解答,题目难度中等.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
 ( )
( )| A、置换反应 | B、水解反应 |
| C、中和反应 | D、电离过程 |
下列属于电解质的是( )
| A、稀硫酸 | B、酒精 | C、铜 | D、小苏打 |
在2A(g)+5B(g)?2C(g)+3D(g)反应中,下列反应速率最快的是( )
| A、υ(A)=0.8 mol/(L?s) |
| B、υ(B)=1.0 mol/(L?s) |
| C、υ(C)=1.8 mol/(L?min) |
| D、υ(D)=0.9 mol/(L?s) |
磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性,制备时将含等物质的量的FeSO4和Fe2(SO4)3的溶液混合,再滴入稍过量的NaOH溶液,随后加入油酸钠溶液,即可生成黑色的、分散质粒子直径在55~36nm的磁流体.下列说法中正确的是( )
| A、所得的分散系属于悬浊液 |
| B、该分散系能产生丁达尔效应 |
| C、所得的分散系中分散质为Fe2O3 |
| D、给分散系通电,不会出现任何变化 |
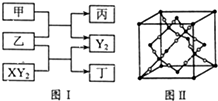 W、X、Y、Z是原子序数依次增大的短周期元素,它们中的两种或三种元素组成化合物甲、乙、丙、丁,几种物质的转化关系如图I所示.常温下0.01mol/L-1丙溶液pH=12;XY2分子是非极性分子,但科学家在特殊条件下制得了XY2的原子晶体,其晶胞结构如图Ⅱ所示.请回答下列问题:
W、X、Y、Z是原子序数依次增大的短周期元素,它们中的两种或三种元素组成化合物甲、乙、丙、丁,几种物质的转化关系如图I所示.常温下0.01mol/L-1丙溶液pH=12;XY2分子是非极性分子,但科学家在特殊条件下制得了XY2的原子晶体,其晶胞结构如图Ⅱ所示.请回答下列问题: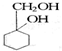 的流程图:
的流程图: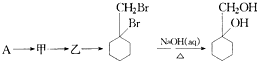
 有多种同分异构体,写出同时符合下列4个条件它的同分异构体的结构简式:
有多种同分异构体,写出同时符合下列4个条件它的同分异构体的结构简式: