题目内容
6.下列反应的离子方程式正确的是( )| A. | 盐酸滴入氨水中:H++OH-═H2O | |
| B. | 碳酸氢铵溶液与足量氢氧化钠溶液混合:HCO3-+OH-═CO32-+H2O | |
| C. | 氢氧化钠溶液中通入过量二氧化硫:SO2+OH-═HSO3- | |
| D. | 碳酸钙溶解于稀硝酸中:CO32-+2H+═CO2↑+H2O |
分析 A.一水合氨为弱碱,应保留化学式;
B.漏掉铵根离子与氢氧根离子的反应;
C.二氧化硫过量,反应生成亚硫酸氢钠;
D.碳酸钙为沉淀,应保留化学式;
解答 解:A.盐酸滴入氨水中,离子方程式:H++NH3•H2O=NH4++H2O,故A错误;
B.碳酸氢铵溶液与足量氢氧化钠溶液混合,离子方程式:NH4++HCO3-+2OH-═CO32-+H2O+NH3•H2O,故B错误;
C.氢氧化钠溶液中通入过量二氧化硫,离子方程式:SO2+OH-═HSO3-,故C正确;
D.碳酸钙溶解于稀硝酸中,离子方程式:CaCO3+2H+═CO2↑+H2O+Ca2+,故D错误;
故选:C.
点评 本题考查了离子方程式,明确反应实质是解题关键,注意化学式的拆分,注意反应物用量对反应产物的影响,题目难度不大.

练习册系列答案
相关题目
16.化学在生产和生活中有着重要的作用.下列说法正确的是( )
| A. | 茂密树林中的道道光柱,既谁一种自然现象又是光学现象,与胶体知识无关 | |
| B. | 焰火的五彩缤纷是某些金属元素化学性质的展现 | |
| C. | “雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮的氧化物无关 | |
| D. | CO2合成聚碳酸酯可降解塑料,以实现“碳”的循环利用 |
17.下列有关化学键的叙述,正确的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 单质分子中均不存在化学键 | |
| C. | 化学键的常见类型为离子键、共价键和氢键 | |
| D. | 离子化合物中一定含有离子键 |
14.根据表中八种短周期元素的有关信息判断,下列说法正确的是( )
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或 最低化合价 | +1 | -2 | +3 | -1 | -2 | +3 | +1 | +1 |
| A. | 元素④气态氢化物的稳定性小于元素⑤气态氢化物的稳定性 | |
| B. | 元素②气态氢化物的沸点小于元素⑤气态氢化物的沸点 | |
| C. | 元素④⑥形成的化合物具有两性 | |
| D. | 元素④⑥⑧的最高价氧化物的水化物两两之间皆能反应 |
1.下列化学用语表达正确的是( )
| A. | HF的电子式为: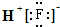 | B. | HClO的结构式:H-Cl-O | ||
| C. | CO2的电子式为: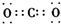 | D. | Cl-的结构示意图: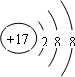 |
18.25℃时,1mol/L醋酸加水稀释至0.01mol/L,下列变化正确的是( )
| A. | 溶液中c(OH-)减小 | B. | pH的变化值小于2 | ||
| C. | 溶液中H+的数目增大 | D. | Kw的值减小 |
15. NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,根据题意回答下列问题:
NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,根据题意回答下列问题:
Ⅰ.利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
2NO(g)+2CO(g) $\stackrel{催化剂}{?}$ 2CO2(g)+N2(g)△H=-748kJ/mol
为了测定某催化剂作用下的反应速率,在一定温度下,向某恒容密闭容器中充入等物质的量的NO和CO发生上述反应.用气体传感器测得不同时间NO浓度如表:
(1)前2s内的平均反应速率υ(N2)=2.08×10-4mol/(L•s)(保留3位有效数字,下同);计算此温度下该反应的K=3.65×106.
(2)达到平衡时,下列措施能提高NO转化率的是BD.(填字母序号)
A.选用更有效的催化剂B.降低反应体系的温度
C.充入氩气使容器内压强增大D.充入CO使容器内压强增大
(3)已知N2(g)+O2(g)=2NO(g)△H=+180kJ/mol;则CO的燃烧热为284kJ/mol.
Ⅱ.臭氧也可用于处理NO.
(4)O3氧化NO结合水洗可产生HNO3和O2,每生成1mol的HNO3转移3mol电子.
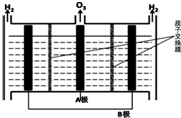
(5)O3可由电解稀硫酸制得,原理如图.图中阴极为B(填“A”或“B”),阳极(惰性电极)的电极反应式为3H2O-6e-=O3+6H+.
 NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,根据题意回答下列问题:
NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,根据题意回答下列问题:Ⅰ.利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
2NO(g)+2CO(g) $\stackrel{催化剂}{?}$ 2CO2(g)+N2(g)△H=-748kJ/mol
为了测定某催化剂作用下的反应速率,在一定温度下,向某恒容密闭容器中充入等物质的量的NO和CO发生上述反应.用气体传感器测得不同时间NO浓度如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | … |
| c(NO)/mol•L-1 | 1.00×10-3 | 4.00×10-4 | 1.70×10-4 | 1.00×10-4 | 1.00×10-4 | … |
(2)达到平衡时,下列措施能提高NO转化率的是BD.(填字母序号)
A.选用更有效的催化剂B.降低反应体系的温度
C.充入氩气使容器内压强增大D.充入CO使容器内压强增大
(3)已知N2(g)+O2(g)=2NO(g)△H=+180kJ/mol;则CO的燃烧热为284kJ/mol.
Ⅱ.臭氧也可用于处理NO.
(4)O3氧化NO结合水洗可产生HNO3和O2,每生成1mol的HNO3转移3mol电子.
(5)O3可由电解稀硫酸制得,原理如图.图中阴极为B(填“A”或“B”),阳极(惰性电极)的电极反应式为3H2O-6e-=O3+6H+.
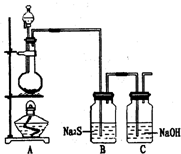 已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题: