题目内容
3.某只含C、H、O三种元素的有机物X的相对分子质量为102,所含氧元素的质量分数为31.4%,则能与Na0H溶液发生反应的X的结构有(不考虑立体异构)( )| A. | 7种 | B. | 9种 | C. | 11种 | D. | 13种 |
分析 某只含C、H、O三种元素的有机物X的相对分子质量为102,所含氧元素的质量分数为31.4%,则分子中N(O)=$\frac{102×31.4%}{16}$=2,分子中碳、氢元素的原子量之和为102-16×2=70,利用余商法$\frac{70}{14}$=5…0,所以分子式为C5H10O2,可能是酸、也可能是酯,酸、酯都可以与碱反应,从而判断同分异构体;
解答 解:某只含C、H、O三种元素的有机物X的相对分子质量为102,所含氧元素的质量分数为31.4%,则分子中N(O)=$\frac{102×31.4%}{16}$=2,分子中碳、氢元素的原子量之和为102-16×2=70,利用余商法$\frac{70}{14}$=5…0,所以分子式为C5H10O2
分子式为C5H10O2的有机物在碱性溶液中发生反应,可能是酸,属于饱和一元酸,
其同分异构体等于丁基的种类,共有4种,
分子式为C5H10O2的有机物在碱性溶液中发生反应,可能是酯,属于饱和一元酯,
若为甲酸和丁醇酯化,丁醇有4种,可形成4种酯;
若为乙酸和丙醇酯化,丙醇有2种,可形成2种酯;
若为丙酸和乙醇酯化,丙酸有1种,可形成1种酯;
若为丁酸和甲醇酯化,丁酸有2种,可形成2种酯;
所以能在碱性溶液中发生反应的C5H10O2的同分异构体有4种羧酸,9种酯,共13种;
故选D.
点评 本题考查有机物分子式的确定、同分异构体书写、官能团的性质等,计算确定有机物的分子式、确定酯的种类是解题的关键,注意掌握官能团的性质.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
13.下列贮存化学试剂的方法正确的是( )
| A. | 浓硝酸保存在棕色的广口瓶中,并放在阴凉处 | |
| B. | 少量的金属钠应保存在煤油中 | |
| C. | 烧碱溶液放在带玻璃塞的磨口试剂瓶中 | |
| D. | 用做感光材料的溴化银贮存在无色试剂瓶中 |
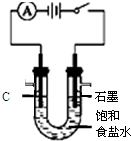
11.用石墨作电极,电解质溶液中各离子浓度之比如下:C(Cu2+):C(Na+):C(Cl-)=1:2:4,在任何情况下,阴、阳两极不可能同时发生的反应是( )
| A. | 阴极:2H++2e-=H2↑ 阳极:4OH--4e-=2H2O+O2↑ | |
| B. | 阴极:Cu2++2e-=Cu 阳极:4OH--4e-=2H2O+O2↑ | |
| C. | 阴极:2H++2e-=H2↑ 阳极:2Cl--2e-=Cl2↑ | |
| D. | 阴极:Cu2++2e-=Cu 阳极:2Cl--2e-=Cl2↑ |
18.在200℃,1个标准大气压下,下列物质完全燃烧体积一定不发生变化的是( )
| A. | CH4、C2H4、C3H4 | |
| B. | CH4、C3H8、C2H2(C2H8、C2H2物质的量之比为1:3) | |
| C. | C2H6、C4H6、C2H2(物质的量之比为2:1:2) | |
| D. | C3H8、C4H8、C2H2(质量之比为11:14:26) |
11.配制一定物质的量浓度的溶液时,如果所配溶液浓度偏小,原因可能是( )
| A. | 转移时没有洗涤2~3次 | |
| B. | 定容时,俯视液面使之与刻度线相平 | |
| C. | 溶解时放出了大量的热,但未等温度恢复为常温就开始转移 | |
| D. | 转移溶液前,容量瓶不干燥,留下少量的水 |
 .
.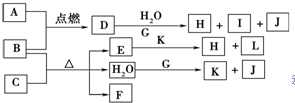 如图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕色烟,B、G为中学化学中常见金属单质,H为红褐色沉淀,I的焰色反应为黄色,组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色.
如图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕色烟,B、G为中学化学中常见金属单质,H为红褐色沉淀,I的焰色反应为黄色,组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色.