题目内容
向明矾溶液中逐滴加入Ba(OH)2溶液至硫酸根离子刚好沉淀完全时,溶液的PH( )
| A、大于7 | B、小于7 |
| C、恰好等于7 | D、上述情况都有可能 |
考点:离子方程式的有关计算
专题:离子反应专题
分析:假设SO42-的物质的量为2mol,则明矾溶液中含有2mol SO42-,1molAl3+,向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-刚好沉淀完全时,需要2molBa(OH)2,即加入的Ba2+为2mol,OH-为4mol,生成2molBaSO4,1molAl3+与4molOH-反应生成1molAlO2-,发生反应:2Ba2++4OH-+Al3++2SO42-+═2BaSO4↓+AlO2-+2H2O,溶液中溶质为KAlO2,根据盐类水解判断溶液pH值.
解答:
解:假设SO42-的物质的量为2mol,则明矾溶液中含有2mol SO42-,1molAl3+,向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-刚好沉淀完全时,需要2molBa(OH)2,即加入的Ba2+为2mol,OH-为4mol,生成2molBaSO4,1molAl3+与4molOH-反应生成1molAlO2-,发生反应:2Ba2++4OH-+Al3++2SO42-+═2BaSO4↓+AlO2-+2H2O,溶液中溶质为KAlO2,AlO2-发生水解,溶液呈碱性,即pH>7,故选A.
点评:本题考查离子方程式及有关计算,难度中等,注意掌握与量有关的离子方程式的书写方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组反应中,第一个反应放出的热量比第二个反应放出的热量多的是(g、l、s分别表示气体、液体、固体)( )
| A、2H2(g)+O2(g)=2H2O(1)2H2(g)+O2(g)=2H2O(g) | ||||
B、
| ||||
C、C(s)+
| ||||
| D、S(s)+O2(g)=SO2(g) S(g)+O2(g)=SO2(g) |
有机化学中取代反应范畴很广,下列反应不属于取代反应的是( )
A、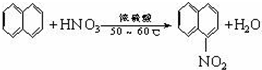 |
B、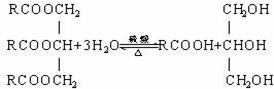 |
C、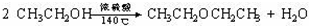 |
D、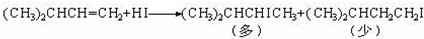 |
可逆反应A(g)+B?C(g)+D,A和C均为无色气体,B和D的聚集状态未知,当反应到达平衡时,下列叙述不正确的是( )
| A、若保持恒容,充入C气体后混合气体颜色加深,则说明B是有颜色的气体 |
| B、若升高温度,发现C的物质的量减少,则说明正反应为放热反应 |
| C、若压缩容器,平衡不移动,则说明B和D一定都是气体 |
| D、保持恒容,到达平衡后继续充入A会使B的转化率增大,A的转化率减少 |
可逆反应2NO2
2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
| △ |
| A、NO2、NO和O2三者共存 |
| B、单位时间内生成n molO2的同时生成2n mol NO |
| C、容器中颜色不再变化 |
| D、容器中NO2、NO、O2的物质的量浓度之比为2:2:1的状态 |
进入2013年以来,我国中东部地区曾出现严重的雾霾天气.下列有关防治雾霾天气的说法不正确的是( )
| A、开发利用太阳能、生物质能等清洁能源 |
| B、研制开发燃料电池汽车 |
| C、积极发展公共交通,倡导绿色出行 |
| D、充分开发利用纯天然纤维,停止使用各种化学合成材料 |
已知分解1mol H2O2放出热量98kJ,在含少量I-的溶液中,H2O2分解的机理为:
H2O2+I-→H2O+IO- 慢
H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法正确的是( )
H2O2+I-→H2O+IO- 慢
H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法正确的是( )
| A、反应速率与I-的浓度有关 |
| B、IO-也是该反应的催化剂 |
| C、反应活化能等于98kJ?mol-1 |
| D、v(H2O2)=v(H2O)=v(O2) |
下列说法中正确的是( )
| A、镀锌铁镀层破损后铁更易被腐蚀 |
| B、当生成物成键释放的总能量大于反应物断键吸收的总能量时,此反应为吸热反应 |
| C、生成物的能量大于反应物的总能量时,反应吸热,△H>0 |
| D、铅蓄电池放电时,Pb作正极,PbO2作负极 |