题目内容
 水是极弱的电解质,改变温度或加入某些电解质会影响水的电离.请回答下列问题:
水是极弱的电解质,改变温度或加入某些电解质会影响水的电离.请回答下列问题:(1)纯水在100℃时,pH=6,该温度下0.1mol?L-1的NaOH溶液中,溶液的pH=
(2)25℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为
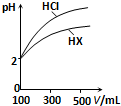
(3)体积均为100mL、pH均为2的盐酸与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX是
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量.
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
②25℃时,在0.5mol/L 的醋酸溶液中由醋酸电离出的c(H+)约是由水电离出的c(H+)的
考点:水的电离,pH的简单计算,离子浓度大小的比较
专题:
分析:(1)先计算出0.1 mol?L-1的NaOH中c(H+),再根据pH=-lg[H+]计算出溶液的pH;
(2)碳酸钠溶液中CO32-部分水解生成碳酸氢根和氢氧根离子,其水解方程式为:CO32-+H2O=HCO3-+OH-;pH=13的碳酸钠溶液中氢离子是由水电离产生的,水电离产生的c(H+)等于溶液中水电离出c(OH -),故水电离出c(OH -)=c(H+)=10-3mol/L;
(3)由图可知,稀释相同倍数时HCl的pH变化大,则酸性HCl>HX;
(4)①根据酸的电离常数进行分析判断,电离常数越大,对应盐的水解程度越小,溶液的pH越小;
②0.5mol/L 的醋酸电离出的c(H+)为
×0.5mol/L,利用Kw来计算水电离产生的氢离子浓度,然后比较即可.
(2)碳酸钠溶液中CO32-部分水解生成碳酸氢根和氢氧根离子,其水解方程式为:CO32-+H2O=HCO3-+OH-;pH=13的碳酸钠溶液中氢离子是由水电离产生的,水电离产生的c(H+)等于溶液中水电离出c(OH -),故水电离出c(OH -)=c(H+)=10-3mol/L;
(3)由图可知,稀释相同倍数时HCl的pH变化大,则酸性HCl>HX;
(4)①根据酸的电离常数进行分析判断,电离常数越大,对应盐的水解程度越小,溶液的pH越小;
②0.5mol/L 的醋酸电离出的c(H+)为
| 1.8×10-5 |
解答:
解:(1)纯水中的[H+]=[OH-],pH=6,[H+]=[OH-]=1×10-6mol?L-1,KW=1×10-6×1×10-6=1×10-12,0.1mol?L-1的NaOH溶液中氢氧根离子浓度为0.1mol/L,c(H+)=1×10-11mol?L-1,pH=-lg[H+]=11,故答案为:11;
(2)碳酸钠溶液中CO32-部分水解生成碳酸氢根和氢氧根离子,其水解方程式为:CO32-+H2O=HCO3-+OH-,pH=13的碳酸钠溶液中氢离子是由水电离产生的,水电离产生的c(H+)等于溶液中水电离出c(OH -),故水电离出c(OH -)=c(H+)=10-3mol/L,故答案为:CO32-+H2O=HCO3-+OH-; 10-3;
(3)由图可知,稀释相同倍数时HCl的pH变化大,则酸性HCl>HX,故HX为弱酸,故答案为:弱酸; 稀释相同倍数,一元酸HX的pH变化量比HCl的小,说明HX存在电离平衡,故HX为弱酸;
(4)①根据图表数据分析,电离常数:醋酸>HCN>碳酸氢根离子,所以等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液水解程度为:Na2CO3>NaCN>CH3COONa,故溶液的pH为:Na2CO3>NaCN>CH3COONa;故答案为:Na2CO3>NaCN>CH3COONa;
②0.5mol/L 的醋酸电离出的c(H+)为
×0.5mol/L,水电离产生的氢离子浓度为
mol/L,则由HAC电离出的c(H+)约为水电离出的c(H+)的9×108故答案为:9×108.
(2)碳酸钠溶液中CO32-部分水解生成碳酸氢根和氢氧根离子,其水解方程式为:CO32-+H2O=HCO3-+OH-,pH=13的碳酸钠溶液中氢离子是由水电离产生的,水电离产生的c(H+)等于溶液中水电离出c(OH -),故水电离出c(OH -)=c(H+)=10-3mol/L,故答案为:CO32-+H2O=HCO3-+OH-; 10-3;
(3)由图可知,稀释相同倍数时HCl的pH变化大,则酸性HCl>HX,故HX为弱酸,故答案为:弱酸; 稀释相同倍数,一元酸HX的pH变化量比HCl的小,说明HX存在电离平衡,故HX为弱酸;
(4)①根据图表数据分析,电离常数:醋酸>HCN>碳酸氢根离子,所以等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液水解程度为:Na2CO3>NaCN>CH3COONa,故溶液的pH为:Na2CO3>NaCN>CH3COONa;故答案为:Na2CO3>NaCN>CH3COONa;
②0.5mol/L 的醋酸电离出的c(H+)为
| 1.8×10-5 |
| 10-14 | ||
|
点评:本题考查盐类水解的应用,溶液酸碱性和pH的计算判断,溶液中离子浓度的大小比较,综合性较强,要注意碳酸是二元弱酸分步电离,第二步电离比HCN小.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
X、Y、Z是3种短周期元素,其中X、Y位于同一族,Y、Z处于同一周期.X原子的外围电子排布式为nSnnPn+2.Z原子的核电荷数是最外层电子数的三倍.下列说法正确的是( )
| A、原子序数由大到小的顺序为Z<Y<X |
| B、Y元素最高价氧化物对应水化物的化学式可表示为H3YO4 |
| C、3种元素的气态氢化物中Z的气态氢化物最稳定 |
| D、原子半径由大到小的顺序为Z>Y>X |
稀溶液一般有依数性,即在一定温度下,相同体积的溶液中溶质粒子数目越多,蒸气压下降数值越大.浓度均为0.1mol?L-1的下列稀溶液,其蒸气压最小的是( )
| A、H2SO3溶液 |
| B、C6H12O6溶液 |
| C、NaCl溶液 |
| D、NH3?H2O溶液 |
分子式是 C8H10 的芳香烃在FeBr3做催化剂的条件下和液溴发生反应,生成的一溴代物有( )种.
| A、5 | B、8 | C、9 | D、10 |
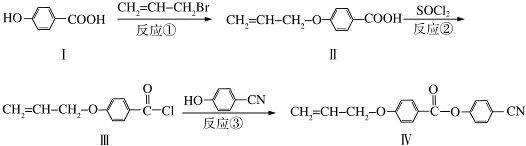
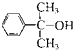 也可与III发生类似反应③的反应生成有机物V,V的结构简式是
也可与III发生类似反应③的反应生成有机物V,V的结构简式是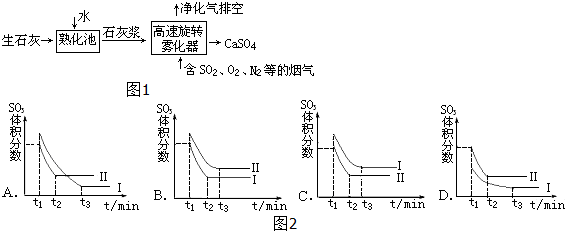
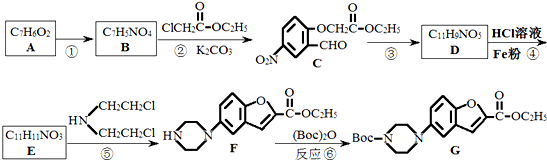
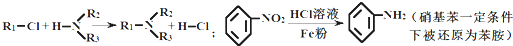
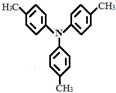 ,请设计合成路线(无机试剂及溶剂任选).
,请设计合成路线(无机试剂及溶剂任选).