��Ŀ����
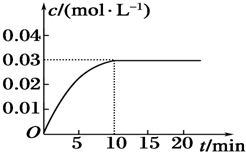
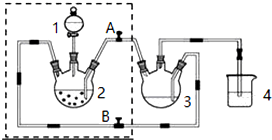
1��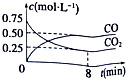 һ�������������Ժ�CO2������Ӧ��Fe��s��+CO2��g��?FeO��s��+CO��g����H��0��1100��ʱ����ij�ܱ������м����������۲�����һ������CO2���壬��Ӧ������CO2�����CO�����Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��
һ�������������Ժ�CO2������Ӧ��Fe��s��+CO2��g��?FeO��s��+CO��g����H��0��1100��ʱ����ij�ܱ������м����������۲�����һ������CO2���壬��Ӧ������CO2�����CO�����Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ����1���÷�Ӧ��ƽ�ⳣ������ʽK=$\frac{c��CO��}{c��C{O}_{2}��}$��
��2�����д�ʩ����ʹƽ��ʱK�������B������ţ���
A�������¶�B������ѹǿC������һ����COD�������¶�
��3��8�����ڣ�CO2��ƽ����Ӧ����v��CO2��=0.0625mol•L-1•min-1��
��4��1100��ʱ��2L���ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�
| ���� | �� | �� |
| ��Ӧ��Ͷ���� | 3mol Fe�� 2mol CO2 | 4mol FeO�� 3mol CO |
| CO��Ũ�ȣ�mol•L-1�� | c1 | c2 |
| CO2��������� | ��1 | ��2 |
| ��ϵѹǿ��Pa�� | p1 | p2 |
| ��̬��Ӧ���ת���� | ��1 | ��2 |
A��p1��p2 B����1=��2 C��2c1=3c2 D����1=��2
����c1=0.67mol•L-1����2=33.3%��
���� ��1����ѧƽ�ⳣ��K����������Ũ����֮���뷴Ӧ��Ũ����֮���ıȵ��������Ӧ��������������Һ��
��2����ѧƽ�ⳣ��ֻ���¶��йأ��뷴Ӧ��Ũ�ȼ�ѹǿ�أ�
��3��8�����ڣ�CO2��ƽ����Ӧ����v��CO2��=$\frac{��c}{��t}$��
��4����A�����º��������£�ѹǿ֮�ȵ�����������ʵ���֮�ȣ�
B���¶Ȳ��仯ѧƽ�ⳣ�����䣬��ѧƽ�ⳣ��K=$\frac{c��CO��}{c��C{O}_{2}��}$��
C�����¶��»�ѧƽ�ⳣ��K=$\frac{0.50}{0.25}$=2
�� Fe��s��+CO2��g��?FeO��s��+CO��g��
��Ӧ��mol/L�� c1 c1
ƽ�⣨mol/L�� 1-c1 c1
��ѧƽ�ⳣ��K=$\frac{{c}_{1}}{1-{c}_{1}}$=2��
�� Fe��s��+CO2��g��?FeO��s��+CO��g��
��Ӧ��mol/L�� 1.5-c2 1.5-c2
ƽ�⣨mol/L�� 1.5-c2 c2
��ѧƽ�ⳣ��K=$\frac{{c}_{2}}{1.5-{c}_{2}}$��
�¶Ȳ��仯ѧƽ�ⳣ�����䣬�ݴ˼���c1��c2��ϵ��
D���� Fe��s��+CO2��g��?FeO��s��+CO��g��
��Ӧ��mol/L�� ��1 ��1
ƽ�⣨mol/L�� 1-��1 ��1
��ѧƽ�ⳣ��K=$\frac{{��}_{1}}{1-{��}_{1}}$
�� Fe��s��+CO2��g��?FeO��s��+CO��g��
��Ӧ��mol/L�� 1.5��2 1.5��2
ƽ�⣨mol/L�� 1.5��2 1.5��1-��2��
��ѧƽ�ⳣ��K=$\frac{1.5��1-{��}_{2}��}{1.5{��}_{2}}$��
�¶Ȳ��仯ѧƽ�ⳣ�����䣬�ݴ˼����1����2��ϵ��
�ڸ��¶��»�ѧƽ�ⳣ��K=$\frac{0.50}{0.25}$=2��K=$\frac{{c}_{1}}{1-{c}_{1}}$=2��K=$\frac{1.5��1-{��}_{2}��}{1.5{��}_{2}}$��
�ݴ˼���c1��a2��
��� �⣺��1����ѧƽ�ⳣ��K����������Ũ����֮���뷴Ӧ��Ũ����֮���ıȵ��������Ӧ��������������Һ�����Ը÷�Ӧ��ѧƽ�ⳣ��K=$\frac{c��CO��}{c��C{O}_{2}��}$��
�ʴ�Ϊ��$\frac{c��CO��}{c��C{O}_{2}��}$��
��2����ѧƽ�ⳣ��ֻ���¶��йأ��뷴Ӧ��Ũ�ȼ�ѹǿ�أ��÷�Ӧ������Ӧ�����ȷ�Ӧ�������¶�ƽ�������ƶ�����ѧƽ�ⳣ��K����ѡB��
��3��8�����ڣ�CO2��ƽ����Ӧ����v��CO2��=$\frac{��c}{��t}$=$\frac{��0.75-0.25��mol/L}{8min}$=0.0625mol/��L��min����
�ʴ�Ϊ��0.0625��
��4����A�����º��������£�ѹǿ֮�ȵ�����������ʵ���֮�ȣ���Ӧǰ������������ʵ������䣬���Լ������������ʵ�����2mol��������3mol�������ѹǿС���ң���p1��p2������ȷ��
B���¶Ȳ��仯ѧƽ�ⳣ�����䣬�ס������¶���ͬ�����Ի�ѧƽ�ⳣ��K=$\frac{c��CO��}{c��C{O}_{2}��}$��ȣ����Ԧ�1=��2������ȷ��
C���� Fe��s��+CO2��g��?FeO��s��+CO��g��
��Ӧ��mol/L�� c1 c1
ƽ�⣨mol/L�� 1-c1 c1
��ѧƽ�ⳣ��K=$\frac{{c}_{1}}{1-{c}_{1}}$
�� Fe��s��+CO2��g��?FeO��s��+CO��g��
��Ӧ��mol/L�� 1.5-c2 1.5-c2
ƽ�⣨mol/L�� 1.5-c2 c2
��ѧƽ�ⳣ��K=$\frac{{c}_{2}}{1.5-{c}_{2}}$��
�¶Ȳ��仯ѧƽ�ⳣ�����䣬����K=$\frac{{c}_{1}}{1-{c}_{1}}$=$\frac{{c}_{2}}{1.5-{c}_{2}}$������3c1=2c2���ʴ���
D�����¶��»�ѧƽ�ⳣ��K=$\frac{0.50}{0.25}$=2
�� Fe��s��+CO2��g��?FeO��s��+CO��g��
��Ӧ��mol/L�� ��1 ��1
ƽ�⣨mol/L�� 1-��1 ��1
��ѧƽ�ⳣ��K=$\frac{{��}_{1}}{1-{��}_{1}}$
�� Fe��s��+CO2��g��?FeO��s��+CO��g��
��Ӧ��mol/L�� 1.5��2 1.5��2
ƽ�⣨mol/L�� 1.5��2 1.5��1-��2��
��ѧƽ�ⳣ��K=$\frac{1.5��1-{��}_{2}��}{1.5{��}_{2}}$��
�¶Ȳ��仯ѧƽ�ⳣ�����䣬����K=$\frac{{��}_{1}}{1-{��}_{1}}$=$\frac{1.5��1-{��}_{2}��}{1.5{��}_{2}}$=2��
���Ԧ�1+��2=1��a1��a2�ֱ�Ϊ$\frac{2}{3}$��$\frac{1}{3}$���ʴ���
�ڸ��¶��»�ѧƽ�ⳣ��K=$\frac{0.50}{0.25}$=2��K=$\frac{{c}_{1}}{1-{c}_{1}}$=2��K=$\frac{1.5��1-{��}_{2}��}{1.5{��}_{2}}$��
c1=0.67mol/L��a2=33.3%��
�ʴ�Ϊ��0.67 mol•L-1��33.3%��
���� ���⿼�黯ѧƽ��Ӱ�����ء���ѧƽ��ļ��㣬���ؿ���ѧ������������������ȷ��ѧƽ�ⳣ��ֻ���¶��йء��¶���ͬ��ѧƽ�ⳣ������ǽⱾ��ؼ���ע�⻯ѧƽ����㷽������Ŀ�Ѷ��еȣ�

 ��У����ϵ�д�
��У����ϵ�д�| A�� | Ag+��Cu2+��NO3-��Na+ | B�� | NO3-��Fe3+��Mg2+��SO42- | ||
| C�� | Na+��Ca2+��Cl-��CO32- | D�� | K+��Ba2+��Cl-��NO3- |
| A�� | ��һ�������£�ij���淴Ӧ���������ȷ�Ӧ������������Ƿ��ȷ�Ӧ | |
| B�� | 1 mol A��ǿ�ᣩ��1 mol B��ǿ������кͷ�Ӧ���ų������������к��� | |
| C�� | ���ε�س��ʱ������ת��Ϊ��ѧ�� | |
| D�� | ��Ҫ���Ȳ��ܷ����ķ�Ӧ���������ȷ�ӦҲ�����Ƿ��ȷ�Ӧ |