题目内容
9.下面有关pH的说法正确的是( )| A. | 在pH=12的溶液中.水电离出的c(OH-)定等于10-12mol/L | |
| B. | 将pH=2和pH=l2的酸碱溶液等体积混合后,溶液的pH一定等于7 | |
| C. | 若强酸、强碱中和后pH=7,则中和之前酸、碱的pH之和一定等于14 | |
| D. | 含等物质的量的HNO3、Na2CO3、CH3COOH的溶液混合后.溶液的pH一定大于7 |
分析 A.室温下,在pH=12的某种溶液呈碱性,可能是碱溶液也可能是强碱弱酸盐溶液,需要根据溶液呈碱性的原因判断;
B.若酸为弱酸,混合液呈酸性,若碱为弱碱,混合液呈碱性;
C.没有告诉酸碱溶液的体积,无法确定中和之前酸、碱的pH之和;
D.反应后溶质为醋酸钠和醋酸钠,醋酸根离子水解,导致溶液呈碱性.
解答 解:A.如果该溶液是碱溶液,水的电离被抑制,溶液中的氢离子全部来自于碱的电离,则溶液则水电离出的氢氧根离子浓度是10-12 mol/L;如果是强碱弱酸盐溶液,水的电离被促进,溶液中的氢氧根是水电离出的全部,则水电离出的氢氧根离子浓度=10-2 mol/L,故A错误;
B.将pH=2和pH=l2的酸碱溶液等体积混合后,需要根据酸碱的类型判断,若强酸强碱混合,溶液的pH=7,若强酸弱碱混合,混合液呈碱性,若强碱弱酸混合,混合液呈酸性,故B错误;
C.若强酸和强碱溶液等体积混合后pH=7,则中和之前酸、碱的pH之和为14,故C错误;
D.含等物质的量的HNO3、Na2CO3、CH3COOH的溶液混合,反应后的生成物为等物质的量的NaNO3和CH3COONa,醋酸根离子部分水解使溶液呈碱性,故D正确;
故选D.
点评 本题考查了溶液pH的计算,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握弱电解质的电离特点,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
6.分子式为C11H16且只有一个取代基的芳香烃的结构共有(不考虑立体异构)( )
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
20.己知:60℃时,KNO3的溶解度为110g.在此温度下,向盛有l00mL水的烧杯中投入101g KNO3后充分搅拌,此烧杯中将会得到( )
| A. | 悬浊液 | B. | 饱和溶液 | ||
| C. | 质量分数约为50%的溶液 | D. | 物质的量浓度为10mol/L的溶液 |
4.若NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 27 mL 4℃的水中所含分子数约为1.5 NA个 | |
| B. | 电解精炼铜时,阳极减少6.4 g,则转移电子数一定是0.2 NA个 | |
| C. | 标准状况下,22.4L乙烯中共价键数目为8 NA | |
| D. | pH=1的硫酸溶液所含的H+数为NA个 |
14.下列属于有机物的是( )
| A. | HCl | B. | CO(NH2)2 | C. | CO2 | D. | H2O |
1.设NA代表阿伏加德罗常数的数值.则下列有关叙述正确的是( )
| A. | 1molFeI2与足量氯气反应时转移的电子数2 NA | |
| B. | 在1L 0.1mol/L的Na2CO3溶液中,阴离子总数小于0.1NA | |
| C. | 7.8g过氧化钠用于呼吸面具中完全反应时转移电子总数为0.1 NA | |
| D. | 将1L 2mol/L的FeCl3溶液加入到沸水中,加热使之完全反应,所得氢氧化铁胶体粒子数为2NA |
18.下列关于化学与环境的叙述中错误的是( )
| A. | 燃煤时鼓入过量的空气可以减少酸雨的产生 | |
| B. | 利用汽车尾气催化装置可将尾气中的NO和CO转化为无害气体 | |
| C. | “煤改气”、“煤改电”等工程有利于减少雾霾 | |
| D. | 工业废气排放之前必须回收处理以防污染大气 |
19.下列热化学方程式中,正确的是( )
| A. | 已知:H2(g)+F2(g)═2HF(g)△H=-546.6 kJ•mol-1,则1 mol氢气与1 mol氟气反应生成2mol 液态氟化氢放出的热量小于546.6 kJ | |
| B. | 500℃、30 MPa下,将0.5 mol N2(g)和1.5 mol H2(g) 置于密闭容器中充分反应生成NH3(g)放热19.3 kJ.其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则H2SO4(aq)+Ca(OH)2(aq)═CaSO4(s)+2H2O(l)△H=2×(-57.3)kJ•mol-1 | |
| D. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 |
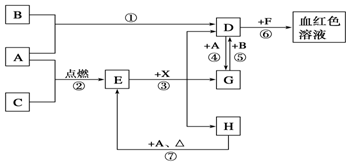 A、B、C为中学常见单质,其中一种为金属,通常情况下,A为固体,B为黄绿色气体,C为无色气体.D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体.它们之间的转化关系如图所示(其中某些反应条件和部分反应物已略去).
A、B、C为中学常见单质,其中一种为金属,通常情况下,A为固体,B为黄绿色气体,C为无色气体.D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体.它们之间的转化关系如图所示(其中某些反应条件和部分反应物已略去).