题目内容
18.某同学在实验室研究Fe与H2SO4的反应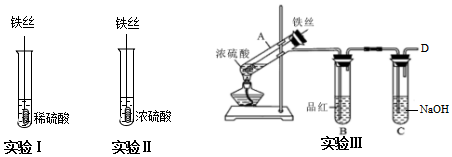
【实验分析】
(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为Fe+2H+=Fe2++H2↑.
(2)实验Ⅱ中,铁丝表面迅速发黑(Fe3O4),有少量气体产生,反应很快停止,
这一现象被称为钝化.
(3)实验Ⅲ,已知:浓H2SO4的沸点为338.2℃,加热试管A,温度保持在250℃~300℃,产生大量气体,B中品红褪色,D处始终未检测到可燃性气体. A中产生的气体是SO2,装置C的作用是吸收SO2防止污染环境.
(4)实验Ⅲ结束后,经检验A中既有Fe3+又有大量Fe2+.
①产生Fe2+的原因可能是Fe+2Fe3+=3Fe2+(写离子方程式).
②若要检验Fe3+和Fe2+,下列试剂可行的是BC(填字母).
A.KSCN、Fe粉B.KSCN、酸性KMnO4溶液C.KSCN、氯水
【实验反思】
(5)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:
①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性源于+6价S元素,稀硫酸的氧化性源于+1价H元素(H+).
②影响反应产物多样性的因素有浓度、温度、反应物的量等.
分析 (1)Fe和稀硫酸反应生成硫酸亚铁和氢气;
(2)浓硫酸具有强氧化性,发生钝化;
(3)根据硫酸沸点高、产生气体使品红褪色和D处始终未检测到可燃性气体可分析;
(4)①Fe+2Fe3+=3Fe2+,故有Fe3+又有大量Fe2+;
②3SCN-+Fe3+=Fe(SCN)3(血红色),5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,2Fe2++Cl2=2Fe3++2Cl-;
(5)①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性表现在+6价的硫元素上,稀硫酸的氧化性表现在+1价的氢元素上;
②影响反应产物多样性的因素有浓度、温度、反应物的量等.
解答 解:(1)Fe和稀硫酸反应生成硫酸亚铁和氢气,离子方程式为Fe+2H+=Fe2++H2↑,
故答案为:Fe+2H+=Fe2++H2↑;
(2)浓硫酸具有强氧化性,生成致密的氧化膜覆盖在Fe的表面,发生钝化,
故答案为:钝化;
(3)硫酸沸点高、产生气体使品红褪色和D处始终未检测到可燃性气体可推断A中产生的气体为SO2,装置C的作用是吸收SO2防止污染环境,
故答案为:SO2;吸收SO2防止污染环境;
(4)①Fe+2Fe3+=3Fe2+,故有Fe3+又有大量Fe2+
故答案为:Fe+2Fe3+=3Fe2+;
②3SCN-+Fe3+=Fe(SCN)3(血红色),5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,2Fe2++Cl2=2Fe3++2Cl-,
故答案为:B C;
(5))①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性表现在+6价的硫元素上,稀硫酸的氧化性表现在+1价的氢(H+)元素上,
故答案为:+6价S元素,+1价H元素(H+);
②影响反应产物多样性的因素有浓度、温度、反应物的量等
故答案为:浓度、温度、反应物的量等.
点评 本题考查了浓硫酸与Fe反应产物的检验,涉及了Fe及其离子的性质,氢气的性质、离子方程式的书写等,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | LiCl | B. | NaCl | C. | KCl | D. | KBr |
| A. | 氢氧化钡溶液与硫酸镁溶液反应:Ba2++SO42-═BaSO4↓ | |
| B. | 向Ca(ClO)2溶液中通入少量二氧化硫:Ca2++2ClO-+H2O+SO2═2HClO+CaSO3↓ | |
| C. | 向氯化铁溶液中通入氨气:Fe3++3OH-═Fe(OH)3↓ | |
| D. | 氧化钠与冷水反应:Na2O+H2O═2Na++2OH- |
| A. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| B. | 合成纤维和光导纤维都是新型有机非金属材料 | |
| C. | “玉不琢不成器”、“百炼方能成钢”发生的均为化学变化 | |
| D. | “火树银花”中的焰火实质上是金属元素的焰色反应 |
| A. | 除去CO2中少量CO:通过灼热的CuO后收集气体 | |
| B. | 除去BaSO4中少量BaCO3:加足量的稀盐酸,过滤、洗涤、干燥 | |
| C. | 除去KCl溶液中的少量MgCl2:加入适量的NaOH溶液,过滤、蒸发、结晶 | |
| D. | 除去Cu中少量CuO:加足量的稀盐酸,过滤、洗涤、干燥 |
| A. | 100g98%的浓硫酸中含有的氢原子数目为2NA | |
| B. | 30g乙酸中含有的碳氢键数目为2NA | |
| C. | 16g16O2中含有的质子数目为10NA | |
| D. | 1mol苯完全转化为环己烷,转移的电子数目为6NA |
| A. | NaCl溶液 | B. | NaOH溶液 | C. | NaHCO3溶液 | D. | NaHSO4溶液 |

| A. | 在除去KCl的过程中必须用到过滤操作 | |
| B. | 在Cl2与KOH反应时,KOH作还原剂 | |
| C. | 在溶液A中加入KOH固体的作用是使KClO3转化为KClO | |
| D. | 在溶液A中加入KOH固体的作用是放出更多的热量,有利于提高反应速率 |
| A. |  | B. |  | C. |  | D. |  |