题目内容
9.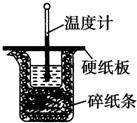 50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:(1)从实验装置上看,图中尚缺少的一种玻璃仪器是环形玻璃搅拌棒.
(2)烧杯间填满碎泡沫塑料的作用是减少实验过程中的热量损失.
(3)理论上稀的强酸溶液与强碱溶液反应生成1mol水时放出57.3kJ的热量,写出表示稀盐酸和稀氢氧化钠溶液反应的中和热的热化学方程式:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ/mol
(4)大烧杯上如不盖硬纸板,求得的中和热数值偏小(填“偏大”、“偏小”或“无影响”).
(5)实验中改用60mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量不相等(填“相等”或“不相等”),所求中和热相等(填“相等”或“不相等”),简述理由:中和热是稀的强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关.
(6)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会偏小(填“偏大”“偏小”或“无影响”).
分析 (1)根据量热计的构造来判断该装置的缺少仪器;
(2)中和热测定实验成败的关键是保温工作;
(3)根据物质的物质的量与热量之间的关系以及热化学方程式的书写方法书写;
(4)不盖硬纸板,会有一部分热量散失;
(5)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;
(6)根据弱电解质电离吸热分析.
解答 解:(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒;
故答案为:环形玻璃搅拌棒;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是减少实验过程中的热量损失,
故答案为:减少实验过程中的热量损失;
(3)稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,稀盐酸和稀氢氧化钠溶液反应的中和热的热化学方程式:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ/mol;
故答案为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ/mol;
(4)大烧杯上如不盖硬纸板,会有一部分热量散失,求得的中和热数值将会减小;
故答案为:偏小;
(5)反应放出的热量和所用酸以及碱的量的多少有关,用60mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液进行反应,与上述实验相比,生成水的量增加,所放出的热量偏高,但是中和热是稀的强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以用60mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液进行反应,测得中和热数值相等;
故答案为:不相等;相等;中和热是稀的强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关;
(6)一水合氨为弱碱,电离过程为吸热过程,所以用氨水代替NaOH溶液反应,反应放出的热量偏小,中和热的数值会偏小;
故答案为:偏小.
点评 本题考查了中和热的测定、误差分析,题目难度不大,注意掌握测定中和热的正确方法,明确实验操作过程中关键在于尽可能减少热量散失,使测定结果更加准确.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案2N2O5(g)?4NO2(g)+O2(g)△H=+Q kJ/mol
一定温度时,向1L密闭容器中通入N2O5,部分实验数据见如表:
| 时间(s) | 0 | 500 | 1000 | 1500 |
| c(N2O5)(mol•L) | 0.50 | 0.35 | 0.25 | 0.25 |
(1)计算前500s NO2的反应速率0.0006mol/(L•s)(不需计算过程)
(2)在一定温度下,该反应1000s时达到平衡,试计算该温度下平衡常数.
(3)在该温度下,如再向该密闭装置中通入0.25mol N2O5和0.375mol O2,请判断此时平衡的移动方向,并计算达平衡后N2O5的体积分数.
| A. | 13C和14C属于同一种元素,也属于同一种核素 | |
| B. | 1H和2H是不同的核素,两者互为同位素 | |
| C. | H2O和D2O互为同素异形体 | |
| D. | 金刚石和石墨都是碳元素形成的单质,具有相同的物理化学性质 |
| A. | 用10mL量筒量取10.1mL盐酸 | |
| B. | 用100mL量筒量取15.2mL盐酸 | |
| C. | 用托盘天平秤取25.20gNaCl | |
| D. | 用100mL容量瓶配制90mL0.10mol/LNaCl溶液 |
| A. | 淀粉和纤维素均可用(C6H10O5)n表示,因此它们互为同分异构体 | |
| B. | 淀粉和纤维素水解的最终产物都能发生银镜反应 | |
| C. | 实验时不小心将浓硝酸滴到皮肤上,皮肤表面会变黄 | |
| D. | 动物脂肪发生皂化反应,能生成甘油和高级脂肪酸钠 |
| A. | 12g金刚石中所含的共价键数为4NA | |
| B. | 标准状况下,11.2L SO3所含的氧原子数为1.5NA | |
| C. | 常温下,1L0.1mol/L的NH4NO3溶液中铵根离子为0.1 NA | |
| D. | 1mol 过氧化氢分解转移NA电子 |
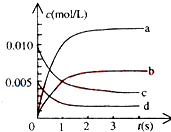 800℃时,在2L密闭容器中发生反应2NO(g)+O2(g)?2NO2(g),在反应体系中,n(NO)随时间的变化如表所示:
800℃时,在2L密闭容器中发生反应2NO(g)+O2(g)?2NO2(g),在反应体系中,n(NO)随时间的变化如表所示:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
②能说明该反应已经达到平衡状态的是bc
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变.
| A. | 福尔马林 | B. | 18.4 mol•L-1的硫酸溶液 | ||
| C. | 饱和Na2SO4溶液 | D. | 1 mol•L-1的CuSO4溶液 |
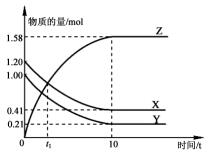 一定温度下,在1L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在1L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 反应开始到10 s,用Z表示的反应速率为0.158 mol/(L•s) | |
| B. | t1时,Z和X的浓度相等,达到了化学平衡状态 | |
| C. | 反应开始到10 s时,Y的正逆反应速率都相等 | |
| D. | 反应的化学方程式为:X(g)+Y(g)?Z(g) |