题目内容
下列反应的离子方程式书写正确的是( )
| A、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+OH-+Ba2+═H2O+BaCO3↓ |
| C、NaHCO3溶液和过量Ba(OH)2溶液混合:2HCO3-+2OH-+Ba2+═BaCO3↓+2H2O+CO32- |
| D、NaAlO2溶液中通入少量CO2:2A1O2-+CO2+3H2O═2Al(OH)3↓+CO32- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氯化铝与氨水反应生成氢氧化铝沉淀,不是生成偏铝酸根离子;
B.氢氧化钡少量,离子方程式按照氢氧化钡的化学式组成书写,碳酸根离子有剩余;
C.氢氧化钡过量,离子方程式按照碳酸氢钠的化学式组成书写,氢氧根离子有剩余;
D.二氧化碳少量,反应生成氢氧化铝沉淀和碳酸钠.
B.氢氧化钡少量,离子方程式按照氢氧化钡的化学式组成书写,碳酸根离子有剩余;
C.氢氧化钡过量,离子方程式按照碳酸氢钠的化学式组成书写,氢氧根离子有剩余;
D.二氧化碳少量,反应生成氢氧化铝沉淀和碳酸钠.
解答:
解:A.氨水碱性较弱,不会溶解氢氧化铝,二者反应生成氢氧化铝和氯化铵,离子反应为Al3++3NH3?H2O═Al(OH)3↓+3NH4+,故A错误;
B.NaHCO3溶液和少量Ba(OH)2溶液混合,碳酸根离子有剩余,正确的离子方程式为:2HCO3-+Ba2++2OH-=BaCO3↓+CO32-+2H2O,故B错误;
C.NaHCO3溶液和过量Ba(OH)2溶液混合,反应生成碳酸钡沉淀和水,正确的离子方程式为:HCO3-+OH-+Ba2+═H2O+BaCO3↓,故C错误;
D.偏铝酸钠溶液中通入少量CO2,碳酸氢根离子的酸性大于偏铝酸根离子,反应生成氢氧化铝沉淀和碳酸钠,反应的离子方程式为:2A1O2-+CO2+3H2O═2Al(OH)3↓+CO32-,故D正确;
故选D.
B.NaHCO3溶液和少量Ba(OH)2溶液混合,碳酸根离子有剩余,正确的离子方程式为:2HCO3-+Ba2++2OH-=BaCO3↓+CO32-+2H2O,故B错误;
C.NaHCO3溶液和过量Ba(OH)2溶液混合,反应生成碳酸钡沉淀和水,正确的离子方程式为:HCO3-+OH-+Ba2+═H2O+BaCO3↓,故C错误;
D.偏铝酸钠溶液中通入少量CO2,碳酸氢根离子的酸性大于偏铝酸根离子,反应生成氢氧化铝沉淀和碳酸钠,反应的离子方程式为:2A1O2-+CO2+3H2O═2Al(OH)3↓+CO32-,故D正确;
故选D.
点评:本题考查了离子方程式书写判断,题目难度中等,注意掌握离子反应发生条件,明确离子方程式的书写原则,试题侧重考查反应物过量情况的考查,正确判断生成物为解答关键.

练习册系列答案
相关题目
下列物质属于化合物的是( )
| A、H2O |
| B、N2 |
| C、Cl2 |
| D、Fe |
 如图中C%表示某反应物在体系中的百分含量,v表示反应速率,P表示压强,t表示反应时间.下图(A)为温度一定时,压强与反应速率的关系曲线;下图(B)为压强一定时,在不同时间C%与温度的关系曲线.同时符合以下两个图象的反应是( )
如图中C%表示某反应物在体系中的百分含量,v表示反应速率,P表示压强,t表示反应时间.下图(A)为温度一定时,压强与反应速率的关系曲线;下图(B)为压强一定时,在不同时间C%与温度的关系曲线.同时符合以下两个图象的反应是( )| A、4NH2(g)+5O2(g)?4NO(g)+6H2O(g)△H=-808.7Kj/mol |
| B、N2O3(g)?NO2(g)+NO(g)△H=+41.8Kj/mol |
| C、3NO2(g)+H2O(l)?2HNO2(l)+NO(g)△H=-261.3Kj/mol |
| D、CO2(g)+C(s)?2CO(g)△H=+171.4Kj/mol |
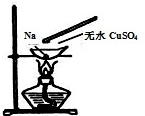 如图,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成.据此判断下列说法中不正确的是( )
如图,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成.据此判断下列说法中不正确的是( )| A、上述反应是置换反应 |
| B、上述反应说明钠比铜活泼 |
| C、上述反应证明钠可以从CuSO4溶液中置换出铜 |
| D、加热且无水条件下,Na可以与CuSO4反应并生成Cu |
常温下,往H2O2溶液滴加少量FeSO4溶液,可发生如下两个反应:下列说法正确的是 ( )
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe3++H2O2=2Fe2++O2↑+2H+.
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe3++H2O2=2Fe2++O2↑+2H+.
| A、H2O2的氧化性比Fe3+强,其还原性比Fe2+弱 |
| B、在H2O2分解过程中,溶液的H+浓度逐渐下降 |
| C、在H2O2分解过程中,Fe2+和Fe3+的总量保持不变 |
| D、H2O2生产过程中往往需要加入少量Fe2+以提高产率 |