题目内容
13.下列现象描述错误的是( )| A. | 氯气与紫色石蕊溶液--先变红后褪色 | |
| B. | 过量的Cl2与KI淀粉溶液--变蓝 | |
| C. | SO2与紫色石蕊溶液--变红 | |
| D. | 硫化氢与湿润的醋酸铅试纸--变黑 |
分析 A、氯气与水反应生成HCl、HClO,溶液具有酸性和漂白性,以此来解答;
B、氯气和次氯酸都具有强氧化性,但氯气没有漂白性、次氯酸有漂白性;
C、酸能使紫色石蕊试液变红色;
D、硫化氢与醋酸铅反应生成黑色硫化铅.
解答 解:A、氯气与水反应生成HCl、HClO,溶液具有酸性和漂白性,则紫色石蕊溶液先变红后褪色,故A正确;
B、氯气和次氯酸都具有强氧化性,但氯气没有漂白性、次氯酸有漂白性,氯气氧化碘离子生成碘,使KI淀粉溶液变蓝,氯气和水反应生成的次氯酸使蓝色褪去,故B错误;
C、二氧化硫与水反应生成亚硫酸,酸能使紫色石蕊试液变红色,故C正确;
D、硫化氢与醋酸铅反应生成黑色硫化铅,故D正确;
故选B.
点评 本题考查氯气的性质,题目难度不大,注意把握氯气与水的反应及氯水具有酸性和漂白性为解答的关键,HClO的漂白性为解答的易错点.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
16.向20mL 2mol/L AlCl3溶液中加入30mL NaOH溶液,充分反应后得到0.78g沉淀,由此可知NaOH溶液的物质的量浓度应该是( )
①1mol/L ②2mol/L ③5mol/L ④8mol/L.
①1mol/L ②2mol/L ③5mol/L ④8mol/L.
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
4.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,2.24 L CCl4含有0.1 NA个CCl4分子 | |
| B. | 18gD2O含有的质子数为10NA | |
| C. | 标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA | |
| D. | 1.5molCu和足量稀硝酸反应产生NA个NO分子 |
1.对下列实验过程的评价,正确的是( )
| A. | 某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐 | |
| B. | 验证溶液中是否含有Cl-,加稀硝酸酸化的AgNO3溶液,有白色沉淀,证明含Cl- | |
| C. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ | |
| D. | 某溶液中滴加盐酸酸化的BaCl2溶液,生成白色沉淀,证明一定含有SO42- |
8.某有机物的结构简式如图所示,下列有关该物质的叙述,正确的是( )
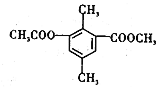

| A. | 分子中不同化学环境的氢共有4种 | |
| B. | 分子中所有的碳原子不可能共平面 | |
| C. | lmol该有机物与足量NaOH溶液反应,最多消耗3mol NaOH | |
| D. | 能发生取代、消去、加成和氧化反应 |
18.分子式为C4H10O的有机物,能与钠反应放出H2的有( )种.
| A. | 4 | B. | 6 | C. | 7 | D. | 8 |
5.如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略).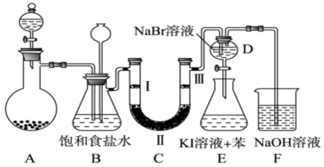
(1)固体二氧化锰和浓盐酸制备氯气的化学反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中锥形瓶水位下降,长颈漏斗中液面上升,形成水柱.
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入d.(填序号)
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱.当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为橙黄色,说明Cl2氧化性>Br2(填>、<或=).打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象是E中溶液分为两层,上层(苯层)为紫红色.
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的化学方程式2NaOH+Cl2=NaCl+NaClO+H2.

(1)固体二氧化锰和浓盐酸制备氯气的化学反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中锥形瓶水位下降,长颈漏斗中液面上升,形成水柱.
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入d.(填序号)
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的化学方程式2NaOH+Cl2=NaCl+NaClO+H2.
2.下列各组中的两种物质互为同分异构体的是( )
| A. | 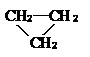 和CH3CH=CH2 和CH3CH=CH2 | B. | 淀粉和纤维素 | ||
| C. | CH3CH2CH2CH3和CH3CH2CH3 | D. | 乙烷和乙酸 |
3.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生.下列属于未来新能源标准的是( )
①太阳能 ②石油 ③风能 ④氢能 ⑤核能 ⑥生物质能 ⑦天然气.
①太阳能 ②石油 ③风能 ④氢能 ⑤核能 ⑥生物质能 ⑦天然气.
| A. | ①③④⑥ | B. | ②③④⑤ | C. | ②④⑥⑦ | D. | ①③⑤⑦ |