题目内容
现有稀盐酸、稀硫酸、氢氧化钡、碳酸钠四瓶失去标签的溶液,分别编号为A、B、C、D.每次取少量溶液两两混合,所观察到现象记录在表中(“-”表示无明显现象;“↓”表示有沉淀生成;“↑”表示有气体生成)
(1)据此推断这四瓶溶液中的溶质分别为:
A ;B ; C ;D ;
(2)写出上述实验过程中有关物质间反应的离子方程式:
A+B ;C+D ;A+C .
(1)据此推断这四瓶溶液中的溶质分别为:
A
(2)写出上述实验过程中有关物质间反应的离子方程式:
| A | B | C | D | |
| A | ↑ | ↓ | - | |
| B | ↑ | ↓ | ↑ | |
| C | ↓ | ↓ | - | |
| D | - | ↑ | - |
考点:无机物的推断
专题:
分析:将所给四种物质两两混合,产生一个气体的是盐酸,一个沉淀一个气体的是硫酸,两个沉淀的是氢氧化钡,两个气体一个沉淀的是碳酸钠,A是一个气体一个沉淀,故A为硫酸;B是两个气体一个沉淀,故B为碳酸钠;C是两个沉淀,C为氢氧化钡;D是一个气体,D为盐酸.
解答:
解:将所给四种物质两两混合,产生一个气体的是盐酸,一个沉淀一个气体的是硫酸,两个沉淀的是氢氧化钡,两个气体一个沉淀的是碳酸钠,A是一个气体一个沉淀,故A为硫酸;B是两个气体一个沉淀,故B为碳酸钠;C是两个沉淀,C为氢氧化钡;D是一个气体,D为盐酸,
(1)由以上分析知A为硫酸,B为碳酸钠,C为氢氧化钡,D为盐酸,故答案为:硫酸;碳酸钠;氢氧化钡;盐酸;
(2)硫酸与碳酸钠反应离子方程式为CO32-+2H+=CO2↑+H2O;
氢氧化钡与盐酸反应离子方程式为OH-+H+=H2O;
硫酸与氢氧化钡反应离子方程式为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O.
(1)由以上分析知A为硫酸,B为碳酸钠,C为氢氧化钡,D为盐酸,故答案为:硫酸;碳酸钠;氢氧化钡;盐酸;
(2)硫酸与碳酸钠反应离子方程式为CO32-+2H+=CO2↑+H2O;
氢氧化钡与盐酸反应离子方程式为OH-+H+=H2O;
硫酸与氢氧化钡反应离子方程式为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O.
点评:本题考查了物质的推断,根据两两混合产生的现象判断即可,熟知各物质的性质是解答的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验操作中错误的是( )
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面 |
| D、称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中(放有等质量的纸) |
下列图示与对应叙述相符合的是( )
A、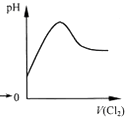 表示Cl2通入SO2溶液中pH的变化 |
B、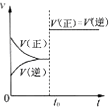 表示已达平衡的某可逆反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂 |
C、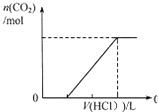 表示在含等物质的量NaOH、Na2CO3的混合溶液中滴加0.1mol?L-1盐酸至过量时,产生气体的体积与消耗盐酸的关系 |
D、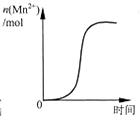 表示10 mL 0.01 mol?L-1KMnO4 酸性溶液与过量的0.1 mol?L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化(Mn2+对该反应有催化作用) |
下列说法正确的是( )
| A、在由水电离产生的氢离子浓度为10-13 mol?L-1的溶液中,Ca2+、K+、Cl-、HCO3-四种离子能大量共存 |
| B、已知MgCO3的Ksp═6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)═6.82×10-6 |
| C、对于反应2N2H4(l)=N2(g)+2H2(g)△H=-50.6 kJ?mol-1,它只在高温下自发进行 |
| D、常温下,将0.2 mol?L-1某一元碱(ROH)溶液和0.1 mol?L-1HCl溶液等体积混合,混合后溶液pH<7,则c(ROH)>c(R+) |
下列溶液中微粒的物质的量浓度关系正确的是( )
| A、1L 0.1mol/L(NH4)2Fe(SO4)2的溶液:c(SO42-)>c(NH4+)>c(Fe2+)>c(OH-)>c(H+) |
| B、在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-) |
| C、常温下,CH3COONa溶液和盐酸混合所得中性溶液:c(Na+)>c(Cl-)=c(CH3COOH) |
| D、25℃时,pH=4.5的NaHC2O4溶液:c(HC2O4-)>c(C2O42-)>c(H2C2O4) |
下列变化中,需要加入氧化剂的是( )
| A、HCl→H2 |
| B、HCl→FeCl2 |
| C、H2SO4(浓)→SO2 |
| D、Fe→Fe2O3 |
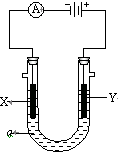 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: