题目内容
氮可以形成多种离子,如N3-、NH2-、N3-、NH4+、N2H5+、N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于NH4+的性质.
(1)NH2-的电子式为 .
(2)N3-有 个电子.
(3)写出两种由多个原子组成的含有与N3-电子数相同的物质的化学式 、 .
(4)等电子数的粒子往往具有相似的结构,试预测N3-的构型 .
(5)据报道,美国科学家卡尔?克里斯特于1998年11月2日合成了一种名为“N5”的物质,由于其极强的爆炸性,又称为“盐粒炸弹”.迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排列成V形.如果5个N结合后都达到8个电子结构,且含有2个氮氮三键,则“N5”分子碎片所带电荷是 .
(1)NH2-的电子式为
(2)N3-有
(3)写出两种由多个原子组成的含有与N3-电子数相同的物质的化学式
(4)等电子数的粒子往往具有相似的结构,试预测N3-的构型
(5)据报道,美国科学家卡尔?克里斯特于1998年11月2日合成了一种名为“N5”的物质,由于其极强的爆炸性,又称为“盐粒炸弹”.迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排列成V形.如果5个N结合后都达到8个电子结构,且含有2个氮氮三键,则“N5”分子碎片所带电荷是
考点:“等电子原理”的应用,判断简单分子或离子的构型
专题:化学键与晶体结构
分析:(1)NH2-的电子式为: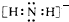 ;
;
(2)1个N含有7个电子,故N3-有22个电子;
(3)含有22个电子的多原子物质有N2O、CO2、CNO-、BeF2、CaH2、C3H4等;
(4)CO2为直线型分子,故可认为N3-的构型为直线型;
(5)N5结构是对称的,5个N排成V形,5个N结合后都达到8电子结构,且含有2个N≡N键,满足条件的结构为: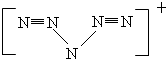 ,故“N5”带一个单位正电荷.
,故“N5”带一个单位正电荷.
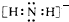 ;
;(2)1个N含有7个电子,故N3-有22个电子;
(3)含有22个电子的多原子物质有N2O、CO2、CNO-、BeF2、CaH2、C3H4等;
(4)CO2为直线型分子,故可认为N3-的构型为直线型;
(5)N5结构是对称的,5个N排成V形,5个N结合后都达到8电子结构,且含有2个N≡N键,满足条件的结构为:
 ,故“N5”带一个单位正电荷.
,故“N5”带一个单位正电荷.解答:
解:(1)NH2-的电子式为: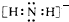 ,故答案为:
,故答案为: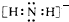 ;
;
(2)1个N含有7个电子,故N3-有22个电子,故答案为:22;
(3)含有22个电子的多原子物质有N2O、CO2、CNO-、BeF2、CaH2、C3H4等,故答案为:N2O、CO2;
(4)CO2为直线型分子,故可认为N3-的构型为直线型,故答案为:直线型;
(5)N5结构是对称的,5个N排成V形,5个N结合后都达到8电子结构,且含有2个N≡N键,满足条件的结构为: ,故“N5”带一个单位正电荷,故答案为:+1.
,故“N5”带一个单位正电荷,故答案为:+1.
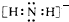 ,故答案为:
,故答案为: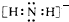 ;
;(2)1个N含有7个电子,故N3-有22个电子,故答案为:22;
(3)含有22个电子的多原子物质有N2O、CO2、CNO-、BeF2、CaH2、C3H4等,故答案为:N2O、CO2;
(4)CO2为直线型分子,故可认为N3-的构型为直线型,故答案为:直线型;
(5)N5结构是对称的,5个N排成V形,5个N结合后都达到8电子结构,且含有2个N≡N键,满足条件的结构为:
 ,故“N5”带一个单位正电荷,故答案为:+1.
,故“N5”带一个单位正电荷,故答案为:+1.
点评:本题重点考查了电子式的书写以及等电子微粒的性质,侧重原子结构与分子构型的分析,注意把握原子的电子排布,题目难度不大.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
在如图装置中,若通电一段时间后乙装置左侧电极质量增加,则下列说法错误的是( )


| A、当甲装置中共产生标准状况下4.48L气体时,Cu电极上质量增加21.6g |
| B、电解过程中装置丙的pH无变化 |
| C、向甲中通人适量的HCl气体,可使溶液恢复到电解前的状态 |
| D、乙中右侧电极反应式:Cu2++2e-═Cu |
 一定温度下,将一定质量的冰醋酸加水稀释的过程中,溶液的导电能力变化如图所示,下列说法中正确的是( )
一定温度下,将一定质量的冰醋酸加水稀释的过程中,溶液的导电能力变化如图所示,下列说法中正确的是( )| A、a,b,c三点溶液的pH:c<a<b |
| B、a,b,c三点醋酸的电离程度:c<a<b |
| C、用湿润的pH试纸测量a处溶液的pH,测量结果偏小 |
| D、a,b,c三点溶液用1 mol?L-1的氢氧化钠溶液中和,消耗氢氧化钠溶液的体积:c<a<b |
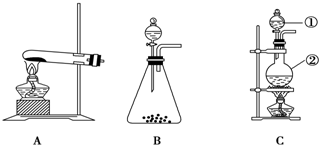
 Sn是人类最早使用的元素之一,能形成SnCl2,SnCl4两种氯化物,SnCl2常温下为白色晶体,具有一维链状的聚合结构,气态时以单分子形式存在,而SnCl4常温下为无色液体.白锡和灰锡是Sn的两种同素异形体,白锡的晶体结构中Sn原子的配位数为4和6,灰锡的晶体结构与金刚石的晶体结构相似.白锡的密度大于灰锡的密度.
Sn是人类最早使用的元素之一,能形成SnCl2,SnCl4两种氯化物,SnCl2常温下为白色晶体,具有一维链状的聚合结构,气态时以单分子形式存在,而SnCl4常温下为无色液体.白锡和灰锡是Sn的两种同素异形体,白锡的晶体结构中Sn原子的配位数为4和6,灰锡的晶体结构与金刚石的晶体结构相似.白锡的密度大于灰锡的密度. 如图所示,烧杯中都盛有稀硫酸.
如图所示,烧杯中都盛有稀硫酸.