题目内容
把0.02mol/LCH3COOH溶液和0.01mol/LNaOH溶液等体积混合后呈酸性,则混合溶液中粒子浓度关系正确的是( )
| A、c(CH3COO-)>c(Na+) |
| B、c(CH3COOH)>c(CH3COO-) |
| C、2c(H+)=c(CH3COO-)-c(CH3COOH) |
| D、c(CH3COOH)+c(CH3COO-)=0.02mol/L |
考点:离子浓度大小的比较,酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:0.02mol/LCH3COOH溶液和0.01mol/LNaOH溶液等体积混合,则实质上是0.05mol/LCH3COOH溶液和0.05mol/LCH3COONa溶液,该溶液显酸性,然后利用电荷守恒及物料守恒等来分析离子浓度的关系.
解答:
解:A、因混合后为0.05mol/LCH3COOH溶液和0.05mol/LCH3COONa溶液,该溶液显酸性,c(H+)>c(OH-),由电荷守恒关系可得c(H+)+c(Na+)=c(CH3COOH-)+c(OH-),则c(CH3COO-)>c(Na+),故A正确;
B、混合后为0.05mol/LCH3COOH溶液和0.05mol/LCH3COONa溶液,酸的电离大于盐的水解,则c(CH3COO-)>c(CH3COOH),故B错误;
C、由电荷守恒c(H+)+c(Na+)=c(CH3COOH-)+c(OH-),物料守恒关系c(CH3COOH)+c(CH3COO-)=2c(Na+),则2c(H+)=(CH3COO-)+2 c(OH-)-c(CH3COOH),故C错误;
D、因混合后为0.05mol/LCH3COOH溶液和0.05mol/LCH3COONa溶液,由物料守恒可知c(CH3COOH)+c(CH3COO-)=c(Na+)×2=0.01mol/L,故D错误;
故选A.
B、混合后为0.05mol/LCH3COOH溶液和0.05mol/LCH3COONa溶液,酸的电离大于盐的水解,则c(CH3COO-)>c(CH3COOH),故B错误;
C、由电荷守恒c(H+)+c(Na+)=c(CH3COOH-)+c(OH-),物料守恒关系c(CH3COOH)+c(CH3COO-)=2c(Na+),则2c(H+)=(CH3COO-)+2 c(OH-)-c(CH3COOH),故C错误;
D、因混合后为0.05mol/LCH3COOH溶液和0.05mol/LCH3COONa溶液,由物料守恒可知c(CH3COOH)+c(CH3COO-)=c(Na+)×2=0.01mol/L,故D错误;
故选A.
点评:本题考查溶液中离子的浓度关系,题目难度中等,明确混合后溶液的溶质是解答的关键,并注意一般酸与盐的混合溶液中溶液显酸性来解答即可,学会合理应用电荷守恒及物料守恒来解题.

练习册系列答案
相关题目
铝合金具有坚硬、轻巧、美观、洁净等特点,可用作门窗等装饰材料,下列与其用途无关的性质是( )
| A、不易生锈 | B、密度小 |
| C、导电性好 | D、强度高 |
一个传热的固定容积的容器中发生反应:mA(g)+nB(g)?pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,一定 能说明达到平衡状态的标志是( )
| A、体系的压强不再改变 |
| B、各组分的浓度不再改变 |
| C、反应速率νA:νB:νC:νD=“m“:n:p:q |
| D、单位时间内m mol A断键发生反应,同时p mol C也断键发生反应 |
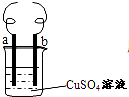 用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解液,如图所示,则下列说法正确的是( )
用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解液,如图所示,则下列说法正确的是( )| A、构成原电池时b极反应式为:Cu2++2e-=Cu |
| B、构成电解池时a极质量一定减少 |
| C、构成电解池时b极质量可能减少也可能增加 |
| D、构成的原电池或电解池工作后,两电极均产生大量气体 |
常温时,有等体积,pH均为2的盐酸和醋酸溶液,下列说法正确的是( )
| A、分别中和等质量的氢氧化钠,消耗盐酸和醋酸溶液的体积相同 |
| B、分别跟足量的镁完全反应,无法比较两者产生氢气的总量大小 |
| C、滴入2滴甲基橙试液后加入等体积的pH=12的Ba(OH)2,溶液仍呈红色 |
| D、分别加水稀释相同的倍数,盐酸中由水电离出的c(H+)比醋酸溶液大 |