题目内容
5.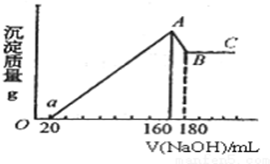 将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.
将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.(1)加入NaOH溶液前20mL时(即Oa段),发生反应的离子方程式为H++OH-=H2O;
(2)A点时,n[Al(OH)3]═0.1mol;
(3)原盐酸溶液中,HCl的物质的量浓度═8mol/L.
分析 根据图象可知,加入20ml氢氧化钠溶液沉淀量不变,说明是氢氧化钠和溶液中盐酸发生的中和反应,a到A是镁离子、铝离子形成氢氧化镁沉淀和氢氧化铝沉淀的过程,A→B是氢氧化钠溶解生成的氢氧化铝,消耗氢氧化钠是20ml,物质的量是0.1mol,则根据方程式Al(OH)3+OH-=AlO2-+2H2O可知氢氧化铝的物质的量是0.1mol.沉淀达到最大值时溶液中的溶质只有氯化钠,此时需要氢氧化钠溶液体积是160ml,物质的量是0.8mol,则氯化钠是0.8mol,根据钠元素守恒此时溶液中n(NaCl)=n(NaOH),据此计算出n(HCl),再利用c=$\frac{n}{V}$计算盐酸的物质的量浓度.
解答 解:(1)加入NaOH溶液前20mL时沉淀量不变,说明是氢氧化钠和溶液中盐酸发生的中和反应,反应的离子方程式为:H++OH-=H2O,
故答案为:H++OH-=H2O;
(2)由图可知,从加入20m氢氧化钠溶液L开始产生沉淀,加入氢氧化钠溶液为160mL时,沉淀量最大,此时为Mg(OH)2和Al(OH)3,再加氢氧化钠,氢氧化铝溶解,由Al(OH)3+NaOH=NaAlO2+2H2O可知,A点的Al(OH)3的物质的量为(180-160)×0.001L×5mol/L=0.1mol,
故答案为:0.1;
(3)加入氢氧化钠溶液为160mL时,沉淀量最大,此时为Mg(OH)2和Al(OH)3,溶液为氯化钠溶液,根据钠元素守恒此时溶液中n(NaCl)=n(NaOH)=0.16L×5mol/L=0.8mol,根据氯元素守恒n(HCl)=0.8mol,故盐酸的物质的量浓度为$\frac{0.8mol}{0.1L}$=8mol/L,
故答案为:8.
点评 本题考查镁铝化合物性质、混合物的计算,以图象题的形式考查,题目难度中等,分析图象各阶段的发生的反应是解题关键,再利用守恒计算.

| A. | 三种元素的原子半径:B最小 | |
| B. | 最高价氧化物对应的水化物:仅B呈碱性 | |
| C. | 常温下,B在A、C的最高价氧化物对应的水化物浓溶液中会发生钝化 | |
| D. | A、B、C的氧化物都是形成酸雨的罪魁祸首 |
| A. | C3H6和C3H8 | B. | C4H6和C3H8 | C. | C5H12和C6H6 | D. | C3H6和C3H8O |
| A. | 27 | B. | 54.1 | C. | 100 | D. | 154 |
| A. | ③④⑤ | B. | ④⑤⑦ | C. | ④⑤ | D. | ③④⑤⑦ |
| A. | 有机物不能通过人工的方法合成 | |
| B. | 烃是指燃烧后只生成CO2和H2O的有机物 | |
| C. | 有机物只含有碳、氢两种元素 | |
| D. | 含碳元素的化合物不一定都属于有机物 |
 ;C 中所含官能团的名称是羧基和溴原子.
;C 中所含官能团的名称是羧基和溴原子. .
.