题目内容
1.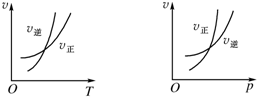 可逆反应mA(g)?nB(g)+pC(g)△H=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是( )
可逆反应mA(g)?nB(g)+pC(g)△H=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是( )| A. | m<n+p,Q>0 | B. | m>n+p,Q>0 | C. | m<n+p,Q<0 | D. | m>n+p,Q<0 |
分析 由图象可知,升高温度,逆反应速率大于正反应速率,则升高温度,平衡逆向移动;增大压强,正反应速率大于逆反应速率,则增大压强,平衡正向移动,以此来解答.
解答 解:由图象可知,升高温度,逆反应速率大于正反应速率,则升高温度,平衡逆向移动,所以该正反应为放热反应,Q<0;
增大压强,正反应速率大于逆反应速率,则增大压强,平衡正向移动,该反应为气体气体缩小的反应,所以m>n+p,
故选D.
点评 本题考查化学平衡及其影响,题目难度不大,利用温度、压强对反应速率的影响分析平衡的移动是解答本题的关键,注意掌握化学平衡的影响因素,试题有利于提高学生的灵活应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g)?3Z(g),平衡时,X、Y、Z的体积分数分别为20%、40%、40%.在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变.下列叙述不正确的是( )
| A. | m=2 | |
| B. | 两次平衡的平衡常数相同,平衡常数值为2 | |
| C. | X与Y的平衡转化率之比为1:1 | |
| D. | 第二次平衡时,Z的浓度为1.0 mol•L-1 |
9.对于可逆反应2SO2(g)+O2(g)?2SO3(g);△H<0,在一恒容容器中,由SO2和O2开始反应,下列说法正确的是( )
| A. | 充入N2,容器内压强增大,增加了单位体积内活化分子数,反应速率加快 | |
| B. | 反应进行的净速率是正、逆反应速率之差 | |
| C. | O2的消耗速率与SO3的生成速率之比为2:1 | |
| D. | 加入SO2,可使单位体积内活化分子百分比增多,加快反应速率 |
16.在一定温度下,NO2和CO在催化剂作用下发生反应4CO(g)+2NO2(g)?N2(g)+4CO2(g)△H<0,当反应达到平衡时,下列措施:①降温 ②恒容通入惰性气体 ③增加NO2浓度 ④加压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高CO转化率的是( )
| A. | ①③④ | B. | ①④⑥ | C. | ②③⑤ | D. | ③⑤⑥ |
13.下列实验操作正确的是( )
| A. | 在2mL10%的氢氧化钠溶液中滴入2%的硫酸铜溶液4~6滴,配制新制氢氧化铜悬浊液,检验醛基 | |
| B. | 实验室制用乙醇与浓硫酸制乙烯时,迅速升温到140℃ | |
| C. | 盛放过苯酚的试剂瓶中残留的苯酚,用水洗涤 | |
| D. | 取加热至亮棕色的纤维素水解液少许,滴入新制的氢氧化铜悬浊液加热,证明水解产物为葡萄糖 |
10.“NaCl+CO2+NH3+H2O→NaHCO3↓+NH4Cl”是著名的“侯氏制碱法”的重要反应.下面是4位同学对该反应涉及的有关知识发表的部分见解.其中不正确的是( )
| A. | 甲同学说:该条件下NaHCO3的溶解度较小 | |
| B. | 乙同学说:NaHCO3不是纯碱 | |
| C. | 丙同学説:析出NaHCO3固体后的溶液中只含氯化铵和氯化钠 | |
| D. | 丁同学说:从该反应可以获得氮肥 |
11.用标准浓度的NaOH溶液滴定未知浓度的盐酸时下列情况会使盐酸物质的量浓度偏低的是( )
| A. | 碱式滴定管用蒸馏水洗净后,直接注入标准浓度的NaOH溶液 | |
| B. | 碱式滴定管尖端有气泡,滴定后气泡消失 | |
| C. | 记录消耗的碱液,滴定前平视,滴定后俯视凹液面 | |
| D. | 锥形瓶用蒸馏水洗净后,直接装入未知浓度的盐酸 |
 .
.