题目内容
3. 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.试回答下列问题:
(1)滴定终点的现象:当滴入最后一滴盐酸时,锥形瓶中的溶液从红色变为无色,且半分钟内不变色
(2)滴定时边滴边摇动锥形瓶,眼睛应观察B
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是用待测溶液润洗锥形瓶由此造成的测定结果偏高(偏高、偏低或无影响)
(4)步骤②缺少的操作是酸式滴定管用蒸馏水洗净后,应用标准液润洗
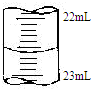
(5)如图是某次滴定时的滴定管中的液面,其读数为22.60mL
(6)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.10 |
分析 (1)滴定终点为锥形瓶中的溶液从红色变为无色时,且半分钟内不变色,应停止滴定;
(2)滴定时眼睛应观察锥形瓶内溶液颜色的变化;
(3)用待测溶液润洗锥形瓶,会使的待测液的物质的量增多;根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析误差;
(4)酸式滴定管用蒸馏水洗净后,应用标准液润洗;
(5)根据滴定管的精确度为0.01mL读数;
(6)根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$计算,V(标准)用两次的平均值.
解答 解:(1)当滴入最后一滴盐酸时,锥形瓶中的溶液从红色变为无色,且半分钟内不变色,达到终点,停止滴定,
故答案为:当滴入最后一滴盐酸时,锥形瓶中的溶液从红色变为无色,且半分钟内不变色;
(2)滴定时眼睛应观察锥形瓶内溶液颜色的变化,
故选答案为:B;
(3)待测溶液润洗锥形瓶,会使的待测液的物质的量增多,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$,可知c(标准)偏大,使测定结果偏高,
故答案为:用待测溶液润洗锥形瓶;偏高;
(4)酸式滴定管用蒸馏水洗净后,应用标准液润洗,否则会使标准液浓度变稀,对测定结果有影响,
故答案为:酸式滴定管用蒸馏水洗净后,应用标准液润洗;
(5)滴定管中的液面读数为22.60mL,
故答案为:22.60;
(6)V(标准)=[(20.40-0.50)+(24.10-4.00)]mL÷2═20.00mL,c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$=$\frac{0.1000mol/L×20.00×1{0}^{-3}L}{25.00×1{0}^{-3}L}$=0.0800mol/L,
故答案为:0.0800.
点评 本题主要考查了中和滴定操作以及注意事项,难度中等,能用c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$准确分析实验误差和计算是解题关键.

 初中学业考试导与练系列答案
初中学业考试导与练系列答案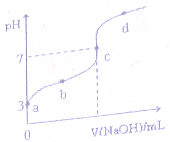 已知常温下CH3COOH的电离平衡常数为 k0,常温下,向20mL 0.1mol•L-1 CH3COOH溶液中逐滴加入0.1mol.L-1NaOH溶液,其 pH变化曲线如图所示(忽略温度变化).下列说法正确的是( )
已知常温下CH3COOH的电离平衡常数为 k0,常温下,向20mL 0.1mol•L-1 CH3COOH溶液中逐滴加入0.1mol.L-1NaOH溶液,其 pH变化曲线如图所示(忽略温度变化).下列说法正确的是( )| A. | a点表溶液中由水电离出的温度为1.0xl0-3mol•L-1 | |
| B. | b 点表示的溶液 c (CH3COO-)<c (Na+) | |
| C. | b、d点表示的溶液中$\frac{c(C{H}_{3}COO)•c({H}^{+})}{c(C{H}_{3}COOH)}$相等 | |
| D. | c点表示CH3COOH和NaOH恰好反应完全 |
| A. | 浓H2SO4 | B. | 稀HNO3 | C. | 盐酸 | D. | CuSO4溶液 |
 实验室以苯甲醛为原料,通过Cannizzaro反应来制备苯甲醇和苯甲酸.反应式如下:
实验室以苯甲醛为原料,通过Cannizzaro反应来制备苯甲醇和苯甲酸.反应式如下: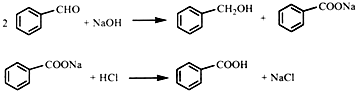
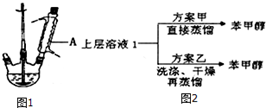
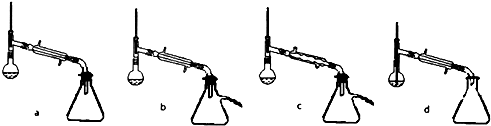
主要反应仪器如图1:
主要物质的物理常数如下表:
| 名称 | 分子量 | 性状 | 相对密度 (g•cm-3) | 熔点 (℃) | 沸点 (℃) | 溶解度 | ||
| 水 | 乙醇 | 乙醚 | ||||||
| 苯甲醛 | 106 | 无色液体 | 1.06 | -26 | 179.6 | 微溶 | 易溶 | 易溶 |
| 苯甲酸 | 122 | 针状结晶 | 1.27 | 122.1 | 249 | 0.21g | 46.6g | 66g |
| 苯甲醇 | 108 | 无色液体 | 1.04 | -15.3 | 205.7 | 微溶 | 易溶 | 易溶 |
| 乙醚 | 74 | 无色液体 | 0.71 | -116.3 | 34.6 | 不溶 | 易溶 | 一 |
①向反应容器中加入5.0g氢氧化钠、10.0mL水和15.0mL苯甲醛.开启搅拌器,加热回流约40min.
②停止加热,向反应物中加入足够量的水,不断摇动,使其中的苯甲酸盐全部溶解.冷却后将反应容器中的液体倒入分液漏斗,加入乙醚进行萃取、分液,得到上层溶液1和下层溶液2.上层溶液1可以经过图2两种方案得到苯甲醇.
③向下层溶液2中加入浓盐酸,并进行操作Ⅰ,得到苯甲酸.
根据以上步骤回答下列问题:
(1)仪器A的名称是球形冷凝管.
(2)上层溶液1蒸馏时先低温蒸出乙醚,蒸馏乙醚时最好采用水浴加热(水浴加热、直接加热.油浴加热).蒸馏操作中,下列装置最好的是b(填标号).
(3)方案乙比方案甲得到的产品纯度更高,方案乙洗涤时先后用到了饱和NaHSO3溶液、10%的Na2CO3溶液和水.
a.饱和NaHSO3溶液的作用是除去苯甲醛.
b.加入10%的Na2CO3溶液至无气泡产生时说明杂质已被除尽.
(4)蒸馏获得苯甲醇操作时温度应控制在205.7℃左右.获得苯甲酸时进行的操作Ⅰ的名称是过滤.
(5)若制得苯甲酸的质量为7.50g.则苯甲酸的产率是81.97%.
 )和抗癫痫药物H(
)和抗癫痫药物H(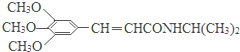 )的路线如图(部分反应略去条件和试剂):
)的路线如图(部分反应略去条件和试剂):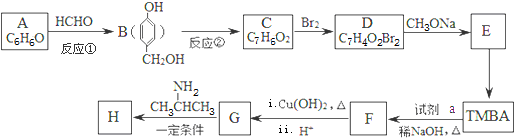
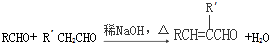 (R、R′表示烃基或氢)
(R、R′表示烃基或氢)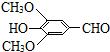 ,试剂a的分子式是C2H4O.
,试剂a的分子式是C2H4O. +2Br2→
+2Br2→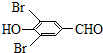 +2HBr.
+2HBr.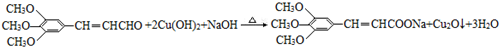 .
.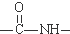 )有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式
)有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 +NaOH→
+NaOH→ +H2NCH(CH3)2.
+H2NCH(CH3)2.