题目内容
高炉炼铁过程中发生的反应:1/3Fe2O3(s)+CO(g) 2/3Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表,下列说法不正确的是
2/3Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表,下列说法不正确的是
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
A.△H<0
B.该反应的平衡常数表达式是
C.其他条件不变,向平衡体系充入CO2气体,K值减小
D.其他条件不变,升高温度,可以降低CO的平衡转化率
C
【解析】
试题分析:A.由于升高温度,化学平衡常数减小,说明升高温度,平衡逆向移动,逆反应方向是吸热反应,所以该反应的正反应是放热反应,所以△H<0,正确;B.化学平衡常数是可逆反应达到平衡状态时生成物的浓度幂之积与反应物浓度幂之积的比。该反应的平衡常数表达式是 ,正确;C.其他条件不变,向平衡体系充入CO2气体,平衡逆向移动,c(CO)、c(CO2)都增大,但是由于温度不变,所以K值不变;D.其他条件不变,升高温度,平衡向吸热的逆反应方向移动,所以CO的平衡转化率降低,正确。
,正确;C.其他条件不变,向平衡体系充入CO2气体,平衡逆向移动,c(CO)、c(CO2)都增大,但是由于温度不变,所以K值不变;D.其他条件不变,升高温度,平衡向吸热的逆反应方向移动,所以CO的平衡转化率降低,正确。
考点:考查化学平衡常数的计算、作用及物质的平衡转化率的计算的知识。

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
 2NH3(g) △H<0,其他条件不变时升高温度,反应速率v(H2)和氢气的平衡转化率均增大
2NH3(g) △H<0,其他条件不变时升高温度,反应速率v(H2)和氢气的平衡转化率均增大 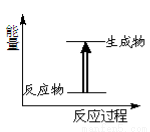
 7N2+12H2O ΔH< 0。请在答题卡的坐标图中,画出上述反应在有催化剂和无催化剂两种情况下反应过程中体系能量变化的示意图,并标明反应热。
7N2+12H2O ΔH< 0。请在答题卡的坐标图中,画出上述反应在有催化剂和无催化剂两种情况下反应过程中体系能量变化的示意图,并标明反应热。
 2SO3(g) ΔH =-196.6 kJ·mol-1
2SO3(g) ΔH =-196.6 kJ·mol-1