题目内容
某研究性学习小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产提取镁,主要过程如下:
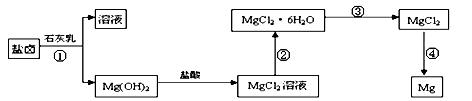
回答下列问题:
(1)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2 ,除去少量Ca(OH)2的方法是先将沉淀加入到盛有 饱和溶液的烧杯中,充分搅拌后经 、 (填操作方法)可得纯净的Mg(OH)2。写出有关反应的离子方程式 。
(2)右图是该研究性学习小组设计进行过程③的实验装置图。其中装置A的作用是 。
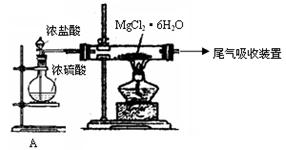
若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是
。
(3)写出过程④中发生反应的化学方程式
。
(1)MgCl2(或氯化镁)(2分) 过滤(2分) 洗涤(2分)
Mg2+ + Ca(OH)2 = Mg(OH)2 + Ca2+ (3分)
(2)制备干燥的HCl气体,抑制MgCl2的水解。(3分)
用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色火焰产生,则证明所得无水氯化镁晶体中不含氯化钠。(2分)(答焰色反应也给分)
(3)MgCl2(熔融) ![]() Mg +Cl2↑(2分)
Mg +Cl2↑(2分)
解析:
略

(12分)海带中含有丰富的碘。为了从海中提取碘,某研究性学习小组设计并进行了以下实验:
请填写下列空白:
⑴步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是 (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
| A.烧杯 | B.坩埚 | C.表面皿 | D.泥三角 E、酒精灯 F、干燥器 |
⑶步骤④反应的离子方程式是 。
⑷步骤⑤中,某学生选择用苯来提取碘的理由是 。
⑸请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法: 。
(06年四川卷)(18分)海带中含有丰富的碘。为了从海中提取碘,某研究性学习小组设计并进行了以下实验:
海带 | ①灼烧 | 海带灰 | ②浸泡 | 海带灰 | ③ | 含碘离子溶液 |
|
|
|
|
| ||||
|
|
|
|
|
|
| H2SO4(稀) |
|
| 单质碘 | ⑥ | 含碘 | ⑤提取碘 | 含碘水溶液 |
|
|
|
|
|
|
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。
(3)步骤④反应的离子方程式是 。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是 。
(5)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法: 。
(06年四川卷)(18分)海带中含有丰富的碘。为了从海中提取碘,某研究性学习小组设计并进行了以下实验:
海带 | ①灼烧 | 海带灰 | ②浸泡 | 海带灰 | ③ | 含碘离子溶液 |
|
|
|
|
| ||||
|
|
|
|
|
|
| H2SO4(稀) |
|
| 单质碘 | ⑥ | 含碘 | ⑤提取碘 | 含碘水溶液 |
|
|
|
|
|
|
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。
(3)步骤④反应的离子方程式是 。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是 。
(5)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法: 。
(06年四川卷)(18分)海带中含有丰富的碘。为了从海中提取碘,某研究性学习小组设计并进行了以下实验:
海带 | ①灼烧 | 海带灰 | ②浸泡 | 海带灰 | ③ | 含碘离子溶液 |
|
|
|
|
| ||||
|
|
|
|
|
|
| H2SO4(稀) |
|
| 单质碘 | ⑥ | 含碘 | ⑤提取碘 | 含碘水溶液 |
|
|
|
|
|
|
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。
(3)步骤④反应的离子方程式是 。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是 。
(5)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法: 。