题目内容
13.某实验中需要90mL0.5mol/L的NaOH溶液,试回答下列问题:(1)若用NaOH固体配制,求需要NaOH多少克.
(2)若用2mol/L的NaOH溶液配制,求需要此溶液多少毫升.
分析 需要90mL0.5mol/L的NaOH溶液,选100mL容量瓶,
(1)结合m=cVM计算;
(2)稀释前后溶质的物质的量不变,以此计算.
解答 解:需要90mL0.5mol/L的NaOH溶液,选100mL容量瓶,
(1)若用NaOH固体配制,需要NaOH为0.1L×0.5mol/L×40g/mol=2.0g,
答:需要NaOH的质量为2.0g;
(2)若用2mol/L的NaOH溶液配制,需要此溶液的体积V=$\frac{0.1L×0.5mol/L}{2mol/L}$=0.025L=25mL,
答:需要此溶液25mL.
点评 本题考查配制一定浓度溶液,为高频考点,把握配制溶液的中容量瓶的选择、物质的量的计算为解答的关键,侧重分析与实验能力的考查,注意容量瓶的选择,题目难度不大.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
5.五种短周期元素在元素周期表中的位置如图所示,其中X元素最高正化合价与最低负化合价的代数和为0,下列判断不正确的是( )
| X | |||||
| Z | Y | M | N |
| A. | N的含氧酸一定是强酸 | B. | 单质Z比单质Y活泼 | ||
| C. | X的原子半径比Y的小 | D. | X和M的原子序数相差10 |
1.下列实验设计与结论不相符的是( )
| A. | 某溶液中加入Ba(NO3)2溶液,再滴加稀盐酸,出现白色沉淀且不溶解,则原溶液中可能含有SO32- | |
| B. | 某气体使湿润的蓝色试纸变红,则该气体一定是酸性氧化物 | |
| C. | 乙醇中混有乙酸,加入氢氧化钠后蒸馏即得纯净的乙醇 | |
| D. | 在分液漏斗中加入溴水,然后加入适量CCl4,振荡后静置,溴可萃取到CCl4中 |
8.下列有关说法正确的是( )
| A. | 2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物种类数相同 | |
| B. | 乙烷、苯、裂化汽油溶液均不能使酸性高锰酸钾溶液褪色 | |
| C. | Na在Cl2中燃烧的生成物含离子键,所以NaCl固体可导电 | |
| D. | 乙醇的沸点比乙酸的沸点低,所以乙醇和乙酸可通过蒸馏初步分离 |
18.海藻中含有丰富的碘元素.如图是实验室从海藻里提取碘的流程的一部分.下列判断正确的是( )
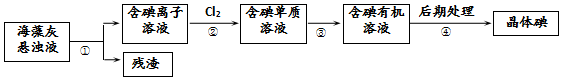

| A. | 步骤④的操作是过滤 | |
| B. | 可用淀粉溶液检验步骤②的反应是否进行完全 | |
| C. | 步骤①、③的操作分别是过滤、萃取 | |
| D. | 步骤③中加入的有机溶剂乙醇 |
5.对于化学反应方向的确定,下列说法正确的是( )
| A. | 固体的溶解过程与焓变有关 | |
| B. | 温度、压强一定时,放热的熵增加反应不一定能自发进行 | |
| C. | 反应焓变是决定反应能否自发进行的唯一因素 | |
| D. | 在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向 |
3.药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
 ,说法正确的是( )
,说法正确的是( )
 ,说法正确的是( )
,说法正确的是( )| A. | 贝诺酯分子中有三种含氧官能团 | |
| B. | 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚 | |
| C. | 乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应 | |
| D. | 贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠 |