题目内容
12.阴离子的中子数为N:AXn-共有x个电子,则N=A-x+n.分析 在阳离子中,核电荷数=质子数=核外电子数+所带电荷数;在阴离子中,核电荷数=质子数=核外电子数-所带电荷数,据此分析.
解答 解:根据在阴离子中:核电荷数=质子数=核外电子数-所带电荷数,即核电荷数=质子数=x-n,又根据质量数=质子数+中子数,即中子数=质量数-质子数=A-(x-n),故答案为:A-x+n.
点评 本题考查了原子结构,题目难度不大,注意把握在阳离子中,核电荷数=质子数=核外电子数+所带电荷数,在阴离子中核电荷数=质子数=核外电子数-所带电荷数.

练习册系列答案
相关题目
19.短周期元素H、X、Y、Z在周期表中的相对位置如图所示.已知X的最高正价和最低负价的代数和为0,下列推断正确的是( )
| X | Y | ||
| H | Z |
| A. | 常温下,含H的两种离子都能使水电离出的c•(H+)•c(OH-)增大 | |
| B. | Y的简单氢化物和Y的最高价含氧酸之间能发生氧化还原反应 | |
| C. | X的气态氢化物的热稳定性比Y的气态氢化物的热稳定性强 | |
| D. | 简单离子半径的大小顺序为H>Z>Y |
7.下列热化学方程式正确的是(注:△H的绝对值均正确)( )
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g);△H=-1367.0 kJ/mol(燃烧热) | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=-57.3kJ/mol(中和热) | |
| C. | S(s)+$\frac{3}{2}$O2(g)═SO3(g);△H=-269.8kJ/mol(反应热) | |
| D. | 2NO2=O2+2NO;△H=+116.2kJ/mol(反应热) |
17.下列分子中,属于非极性分子的是( )
| A. | SO2 | B. | BeCl2 | C. | CH3Cl | D. | COCl2 |
2.下列说法正确的是( )
| A. | CO2无毒,对大气不造成污染,所以可以无限量排放 | |
| B. | NaHCO3比Na2CO3稳定 | |
| C. | Na2CO3溶液可与Ba(OH)2溶液反应,NaHCO3溶液不与Ba(OH)2溶液反应 | |
| D. | NaHCO3溶液与NaOH溶液混合会发生反应,但观察不到明显的现象 |
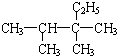 2,3,3-三甲基戊烷 (6)
2,3,3-三甲基戊烷 (6)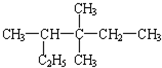 3,3,4-三甲基己烷.
3,3,4-三甲基己烷.