题目内容
用惰性电极电解2L、1mol/L的CuSO4溶液,在电路中通过0.5mol电子后,调换正、负极,电路中又通过了1mol电子,此时溶液中H+的浓度(假设溶液体积不变)是( )
| A、1.5mol/L |
| B、0.75mol/L |
| C、0.5mol/L |
| D、0.25mol/L |
考点:电解原理
专题:电化学专题
分析:调换正负极前后电极反应式如下:调换前:阳极:4OH--4e-=2H2O+O2↑;阴极:2Cu2++4e-=2Cu,
调换后:阳极:2Cu-4e-=2Cu2+(先),4OH--4e-=2H2O+O2↑(后);阴极:2Cu2++4e-=2Cu,
故电路中转移的1.5mol电子中,只有1mol由OH-放电产生,即消耗的n(OH-)=1mol,亦即溶液中积累的n(H+)=1 mol,则c(H+)=0.5mo1?L-1.
调换后:阳极:2Cu-4e-=2Cu2+(先),4OH--4e-=2H2O+O2↑(后);阴极:2Cu2++4e-=2Cu,
故电路中转移的1.5mol电子中,只有1mol由OH-放电产生,即消耗的n(OH-)=1mol,亦即溶液中积累的n(H+)=1 mol,则c(H+)=0.5mo1?L-1.
解答:
解:调换正负极前后电极反应式如下:调换前:阳极:4OH--4e-=2H2O+O2↑;阴极:2Cu2++4e-=2Cu,
用惰性电极电解2L1mol/L的CuSO4溶液,分别是 Cu2+和OH-放电,通过0.5mole-,那么0.25molCu2+放电,生成0.25molCu,同时 4OH--4e-=2H2O+O2↑,反应0.5molOH-,得到0.5molH+,
调换后:阳极:2Cu-4e-=2Cu2+(先),4OH--4e-=2H2O+O2↑(后);阴极:2Cu2++4e-=2Cu,
调换正负极,那么通电前的0.5mole-,恰好是电镀铜的过程,也就是第一个过程的Cu又溶解,在另一电极变为Cu,消耗0.5mole-,剩余0.5mole-,还是得到相同的0.5molH+,
故电路中转移的1.5mol电子中,只有1mol由OH-放电产生,所以总共得到1molH+,
浓度为0.5mol/L.
故选C.
用惰性电极电解2L1mol/L的CuSO4溶液,分别是 Cu2+和OH-放电,通过0.5mole-,那么0.25molCu2+放电,生成0.25molCu,同时 4OH--4e-=2H2O+O2↑,反应0.5molOH-,得到0.5molH+,
调换后:阳极:2Cu-4e-=2Cu2+(先),4OH--4e-=2H2O+O2↑(后);阴极:2Cu2++4e-=2Cu,
调换正负极,那么通电前的0.5mole-,恰好是电镀铜的过程,也就是第一个过程的Cu又溶解,在另一电极变为Cu,消耗0.5mole-,剩余0.5mole-,还是得到相同的0.5molH+,
故电路中转移的1.5mol电子中,只有1mol由OH-放电产生,所以总共得到1molH+,
浓度为0.5mol/L.
故选C.
点评:本题考查电解原理,题目难度中等,本题注意分析调换正负极前后电极反应的变化,为解答该题的关键.

练习册系列答案
相关题目
100mL 2mol/L的硫酸和过量的锌反应,为加快反应速率,但又不影响生成氢气的总量,可采取的措施是( )
| A、升高温度 |
| B、改用含有少量杂质铜的锌 |
| C、改用98%的浓硫酸 |
| D、加水 |
下列比较中,正确的是( )
| A、物质的量浓度相等的醋酸溶液和氢氧化钠溶液等体积混合:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)+c(CH3COOH) |
| B、0.2mol/L NH4NO3和0.1 mol/L NaOH溶液等体积混合后:c(NH4+)>c(NO3-)>c(Na+)>c(OH-)>c(H+) |
| C、常温下,同浓度的一元酸HA比HB易电离,则相同浓度的NaA溶液比NaB溶液的pH大 |
| D、同浓度的下列溶液:①NH4Al(SO4)2 ②NH4Cl ③NH3?H2O ④CH3COONH4,其中c(NH4+)由大到小的顺序是:①>②>④>③ |
下列物质中属于强电解质的是( )
| A、碳酸钠 |
| B、醋酸 |
| C、CO2 |
| D、NaOH溶液 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、通入足量CO2后的溶液中:Na+、SiO32-、C6H5O-、CH3COO- | ||
B、
| ||
| C、pH=0的溶液:Al3+、Ag(NH3)2+、Cl-、SO42- | ||
| D、c(ClO-)=1.0 mol?L-1的溶液:Na+、SO32-、S2-、SO42- |
FeCl3溶液、Fe(OH)3胶体共同具备的性质是( )
| A、都呈透明的红褐色 |
| B、都比较稳定,密封保存一段时间都不会产生沉淀 |
| C、分散质颗粒直径相同 |
| D、当有光线透过时,都能产生丁达尔效应 |
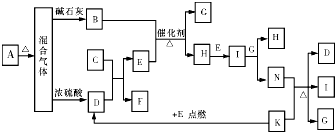 如图中的B~K分别代表有关反应的一种反应物或生成物,其中A、C、F、K是固体;E是常见的气体单质,I是红棕色的气态氧化物.固态物质A(混合物)加热后生成的气体混合物若通过碱石灰只剩余气体B,若通过浓硫酸则只剩余气体D.各物质间的转化关系如图所示.请回答下列问题:
如图中的B~K分别代表有关反应的一种反应物或生成物,其中A、C、F、K是固体;E是常见的气体单质,I是红棕色的气态氧化物.固态物质A(混合物)加热后生成的气体混合物若通过碱石灰只剩余气体B,若通过浓硫酸则只剩余气体D.各物质间的转化关系如图所示.请回答下列问题: