题目内容
 制取氨气并完成喷泉实验(图中夹持装置均已略去).
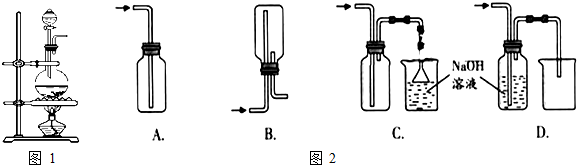
制取氨气并完成喷泉实验(图中夹持装置均已略去).(1)写出实验室制取氨气化学方程式
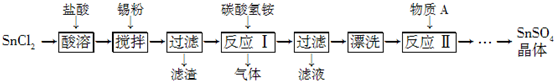
(2)收集氨气应使用
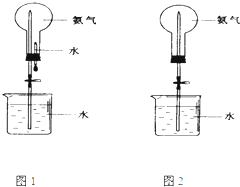
(3)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是
(4)如果只提供如图2的装置,
考点:氨的制取和性质
专题:实验题
分析:(1)氯化铵与氢氧化钙反应生成氯化钙、氨气和水;根据中心原子价层电子对互斥理论确定其空间构型,中心原子含有4个价层电子对,而且含有1个孤电子对的分子为三角锥形;同种非金属元素形成的共价键为非极性共价键,不同种元素之间形成共价键为极性共价键;正负电荷重心重合的分子是非极性分子,正负电荷重心不重合的是极性分子;氨水中的一水合氨为弱电解质,电离产生氨根离子与氢氧根离子;
(2)依据氨气密度小于空气,极易溶于水,属于碱性气体解答;
(3)喷泉实验利用的原理是存在压强差;
(4)喷泉实验需形成明显的压力差,通过加热圆底烧瓶,排除部分氨气,使其溶于水形成压强差.
(2)依据氨气密度小于空气,极易溶于水,属于碱性气体解答;
(3)喷泉实验利用的原理是存在压强差;
(4)喷泉实验需形成明显的压力差,通过加热圆底烧瓶,排除部分氨气,使其溶于水形成压强差.
解答:
解:(1)氯化铵与氢氧化钙反应生成氯化钙、氨气和水,化学方程式为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,氨气分子是N与H形成的极性共价键形成的分子,正负电荷重心不重合,是极性分子,氨水中的一水合氨为弱电解质存在电离:NH3?H2O NH4++OH-,所有氨水显碱性;
故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;极性;极性;NH3?H2O NH4++OH-;
(2)氨气是一种密度小于空气密度,极易溶于水的气体,应选择向下排空气法收集;氨气为碱性气体,应选择碱石灰等碱性干燥剂;氨气为碱性气体遇到湿润的红色石蕊试纸能够使其变蓝;
故答案为:向下排空气法;碱石灰;湿润的红色石蕊试纸靠近集气瓶口看是否变蓝;
(3)氨气是一种极易溶于水的气体,将胶头滴管中的水挤入烧瓶中,瓶内压强减小,在外界气压的作用下,水被压到瓶内,形成喷泉现象,
故答案为:打开止水夹,挤出胶头滴管中的水;氨气极易溶解于水,致使烧瓶内气体压强迅速减小;
(4)氨气是一种极易溶于水的气体,打开夹子,用手(或热毛巾等)将烧瓶捂热,部分氨气溶于水形成压强差,在外界气压的作用下,水被压到瓶内,形成喷泉现象,
故答案为:能;打开夹子,用手(或热毛巾等)将烧瓶捂热.
| ||
故答案为:2NH4Cl+Ca(OH)2
| ||
(2)氨气是一种密度小于空气密度,极易溶于水的气体,应选择向下排空气法收集;氨气为碱性气体,应选择碱石灰等碱性干燥剂;氨气为碱性气体遇到湿润的红色石蕊试纸能够使其变蓝;
故答案为:向下排空气法;碱石灰;湿润的红色石蕊试纸靠近集气瓶口看是否变蓝;
(3)氨气是一种极易溶于水的气体,将胶头滴管中的水挤入烧瓶中,瓶内压强减小,在外界气压的作用下,水被压到瓶内,形成喷泉现象,
故答案为:打开止水夹,挤出胶头滴管中的水;氨气极易溶解于水,致使烧瓶内气体压强迅速减小;
(4)氨气是一种极易溶于水的气体,打开夹子,用手(或热毛巾等)将烧瓶捂热,部分氨气溶于水形成压强差,在外界气压的作用下,水被压到瓶内,形成喷泉现象,
故答案为:能;打开夹子,用手(或热毛巾等)将烧瓶捂热.
点评:本题考查了氨气的实验室制备、氨气的结构及其性质,探究了喷泉的形成,难度不大,熟悉物质的结构和性质是解题关键,注意喷泉实验的原理.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
下列离子方程式正确的是( )
| A、铁和硝酸银溶液反应:Fe+Ag+=Ag+Fe3+ |
| B、氢氧化镁与硫酸溶液反应:H++OH-=H2O |
| C、碳酸钙与醋酸溶液反应:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
| D、铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
 如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g)+3B(g)?2C(g)△H=-192kJ?mol-1.向M、N中,分别通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )
如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g)+3B(g)?2C(g)△H=-192kJ?mol-1.向M、N中,分别通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )| A、若平衡时A气体在两容器中的体积分数相等,则x一定等于y |
| B、若x:y=1:2,则平衡时,M中的转化率:A>B |
| C、若x:y=1:3,当M中放出热量172.8 kJ时,A的转化率为90% |
| D、若x=1.4,y=1,N中达到平衡时体积为2L,C为0.4mol,则反应起始时N的体积为2.6L |
下列应急措施不可取的是( )
| A、被马蜂(其体内分泌物含蚁酸,呈酸性)蜇过的部位,涂些肥皂水可减轻红肿、疼痛 |
| B、误食重金属盐者,立即喝足量牛奶或豆浆或鸡蛋清以紧急解毒 |
| C、锅里油失火时,立即甲油泼掉或加水浇灭 |
| D、酒精灯着火,应立即有湿抹布覆盖酒精灯 |