题目内容
5.依据下列物质的转化关系图,填写以下空格.
(1)A的化学式为O2;C的化学名称为氢氧化铁.
(2)溶液B中一定含有的阴离子是AlO2-.Cl-;
(3)产生气体A的化学方程式为:2Na2O2+2H2O═4NaOH+O2↑.
分析 过氧化钠与水反应生成氢氧化钠和氧气,生成的气体为氧气,氢氧化钠与氯化铁反应生成氢氧化铁,为红褐色沉淀,氢氧化钠与氧化铝反应生成偏铝酸钠,以此解答该题.
解答 解:过氧化钠与水反应生成氢氧化钠和氧气,生成的气体为氧气,氢氧化钠与氯化铁反应生成氢氧化铁,为红褐色沉淀,氢氧化钠与氧化铝反应生成偏铝酸钠,
(1)由以上分析可知A为O2,C为氢氧化铁,故答案为:O2;氢氧化铁;
(2)反应生成偏铝酸钠和氯化钠,二者都溶于水,溶液中含有的阴离子为AlO2-.Cl-,故答案为:AlO2-.Cl-;
(3)过氧化钠和水反应的方程式为2Na2O2+2H2O═4NaOH+O2↑,故答案为:2Na2O2+2H2O═4NaOH+O2↑.
点评 本题以“无机框图题”的形式考查元素单质及其化合物的性质,涉及常用化学用语、化学方程式的书写等,为高频考点,难度不大,在熟练掌握元素化合物知识的基础上着重考查学生的发散思维、分析判断、逻辑思维以及对无机物知识的综合应用等能力.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案
相关题目
15.下列配制物质的量浓度的溶液操作中,会导致实验结果偏低的是( )
| A. | 定容时不慎使液面超过刻度 | |
| B. | 容量瓶中有少量的水,配制前未进行干燥处理 | |
| C. | 未将洗涤玻璃棒和烧杯的洗涤液转入容量瓶中 | |
| D. | 定容时,俯视看刻度 |
16.某1L溶液中含有大量的Cl-、Br-、I-,若向1L该溶液中通入一定量的氯气,溶液中Cl-、Br-、I-的物质的量与通入的氯气的体积(标准状况)的量关系如表所示,分析后判断下列说法正确的是( )
| V(Cl2)(标况,L) | 2.8 | 5.6 | 11.2 |
| n(Cl-) mol | 1.5 | 1.75 | 2.25 |
| n(Br-) mol | 1.5 | 1.4 | 0.9 |
| n(I-)mol | a | 0 | 0 |
| A. | 当通入氯气的体积为2.8L时,溶液中发生的离子反应式只有:Cl2+2I-═2Cl-+I2 | |
| B. | 表中a的值为0.5 | |
| C. | 原溶液中Cl-、Br-、I-物质的量之比为15:15:8 | |
| D. | 原溶液中I-的物质的量浓度为0.25mol/L |
20.设NA代表阿伏加德罗常数,下列说法中,正确的是( )
| A. | 2.7g金属铝变成铝离子时失去的电子数目为0.1NA(提示:M(Al)=27g/mol) | |
| B. | 17g氨气所含的电子数目为10NA(提示:M(NH3)=17g/mol) | |
| C. | 2g氢气所含原子数目为NA(提示:M(H2)=2g/mol) | |
| D. | 常温常压下,11.2L氮气所含的原子数目为NA |
10.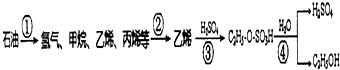 以石油为原料制备乙醇的转化流程图如下所示:跟如图流程图相关的说法中正确的是( )
以石油为原料制备乙醇的转化流程图如下所示:跟如图流程图相关的说法中正确的是( )
 以石油为原料制备乙醇的转化流程图如下所示:跟如图流程图相关的说法中正确的是( )
以石油为原料制备乙醇的转化流程图如下所示:跟如图流程图相关的说法中正确的是( )| A. | 流程图①中产物均为烃类,产物均为可燃性气体 | |
| B. | 流程图①中需减压分馏,②中需分馏分离出乙烯 | |
| C. | 流程图③中发生加成反应,④中发生取代反应 | |
| D. | 乙醇、硫酸都能够使蛋白质变性,都可用于皮肤消毒 |
17.煅烧硫铁矿石(主要成分是FeS2),可获得制取硫酸所需的SO2,反应方程式为:4FeS2+11O2=2Fe2O3+8SO2,为了提高SO2的生成速率,下列措施可行的( )
| A. | 增加硫铁矿石的投入量 | B. | 增加炉的高度 | ||
| C. | 降低温度 | D. | 升高温度 |
14.现有甲、乙两种易溶于水的化合物,已知甲的水溶液不导电,乙的水溶液能导电,下列有关说法正确的是( )
| A. | 甲一定是共价化合物,乙一定是离子化合物 | |
| B. | 甲一定是共价化合物,乙可能是共价化合物 | |
| C. | 甲可能是离子化合物,乙可能是共价化合物 | |
| D. | 甲一定是离子化合物,乙可能是共价化合物 |
10.C、Cl、S、Ti、Fe、Cr元素的单质和化合物的应用研究是目前科学研究的前沿之一,请回答下列问题.
(1)Ti(BH4)2是一种重要的储氢材料.在基态Ti2+中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9.
(2)CH4中共用电子对偏向C,SiH4中硅元素为+4价,则C、Si、H的电负性由大到小的顺序为C>H>Si.
(3)①甲醇(CH3OH)分子内的O-C-H键角小于(填“大于”、“等于”或“小于”)甲醛(H2C═O)分子内的O-C-H键角.
②ClO2-中心氯原子的杂化轨道类型为,写出CN-的等电子体的分子式N2(写出1个).
③石墨烯的应用为电子行业的发展带来了重大的突破,其结构可以看作是单层的石墨,其中碳原子的杂化方式为sp2;
(4)根据表中的数据回答问题
①若只考虑相对分子质量,甲醇的沸点应低于-78.2,甲醇沸点高的原因是甲醇分子之间可以形成氢键
②1mol丙烯中所含σ键和π键数目之比为8:1
③一氟甲烷的空间构型为四面体型.
(1)Ti(BH4)2是一种重要的储氢材料.在基态Ti2+中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9.
(2)CH4中共用电子对偏向C,SiH4中硅元素为+4价,则C、Si、H的电负性由大到小的顺序为C>H>Si.
(3)①甲醇(CH3OH)分子内的O-C-H键角小于(填“大于”、“等于”或“小于”)甲醛(H2C═O)分子内的O-C-H键角.
②ClO2-中心氯原子的杂化轨道类型为,写出CN-的等电子体的分子式N2(写出1个).
③石墨烯的应用为电子行业的发展带来了重大的突破,其结构可以看作是单层的石墨,其中碳原子的杂化方式为sp2;
(4)根据表中的数据回答问题
| 有机物 | 甲醇(CH3OH) | 丙烯(CH3CH=CH2) | 一氟甲烷(CH3F) |
| 相对分子质量 | 32 | 42 | 34 |
| 沸点/℃ | 64.7 | -47.4 | -78.2 |
②1mol丙烯中所含σ键和π键数目之比为8:1
③一氟甲烷的空间构型为四面体型.