题目内容
15.写出CH4与Cl2在光照条件下的反应:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl、CH3Cl+Cl2$\stackrel{光照}{→}$CH2Cl2+HCl、CH2Cl2+Cl2$\stackrel{光照}{→}$CHCl3+HCl、CHCl3+Cl2$\stackrel{光照}{→}$CCl4+HCl.分析 光照条件下,CH4与足量氯气充分反应发生的反应方程式有CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl、CH3Cl+Cl2$\stackrel{光照}{→}$CH2Cl2+HCl、CH2Cl2+Cl2$\stackrel{光照}{→}$CHCl3+HCl、CHCl3+Cl2$\stackrel{光照}{→}$CCl4+HCl,据此分析解答.
解答 解:光照条件下,CH4与足量氯气充分反应发生的反应方程式有CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl、CH3Cl+Cl2$\stackrel{光照}{→}$CH2Cl2+HCl、CH2Cl2+Cl2$\stackrel{光照}{→}$CHCl3+HCl、CHCl3+Cl2$\stackrel{光照}{→}$CCl4+HCl,且每一步中都生成HCl,这几个反应都是取代反应,故答案为:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl;CH3Cl+Cl2$\stackrel{光照}{→}$CH2Cl2+HCl;CH2Cl2+Cl2$\stackrel{光照}{→}$CHCl3+HCl;CHCl3+Cl2$\stackrel{光照}{→}$CCl4+HCl.
点评 本题以甲烷的取代反应为载体考查化学反应方程式的书写,为高频考点,明确取代反应特点是解本题关键,注意反应中H原子个数与氯气分子个数关系,题目难度不大.

练习册系列答案
相关题目
5.下列说法正确的是( )
| A. | 在101kPa下氢气的燃烧热△H=-285.5kJ•mol-1,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| B. | pH=3和pH=5的盐酸各10mL混合,所得溶液的pH=4 | |
| C. | 一定温度下,1L0.50mol/LNH4Cl溶液与2L0.25NH4Cl溶液含NH4+物质的是不同 | |
| D. | 吸热反应“TiO2(g)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0 |
3.下列反应的离子方程式中,书写正确的是( )
| A. | 实验室用大理石跟稀盐酸制取二氧化碳:2H++CO32-═CO2↑+H2O | |
| B. | 氯化铝中加入氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 铁粉与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| D. | 硫酸铜与氢氧化钡溶液反应:Cu2++SO42-+Ba2++2OH-═Cu(OH)2↓+BaSO4↓ |
10.下列各物质中含氮原子数最少的是( )
| A. | 0.1mol NH4Cl | B. | 0.1 mol N2 | ||
| C. | 1.204×1022个CO(NH2)2 | D. | 0.2mol NH3•H2O |
8.化学与生活密切相关,下列叙述正确的是( )
| A. | 光纤通信使用的光缆主要成分是Si,太阳能电池使用的材料主要是SiO2 | |
| B. | 点燃爆竹后,硫燃烧生产SO3 | |
| C. | 海水中含有溴元素,只进行物理变化就可以得到溴单质 | |
| D. | “地沟油”禁止使用,但可以用来制取肥皂 |
9.在恒温恒容的容器中进行反应2A(g)?B(g),若反应物的浓度由0.1mol/L降到0.06mol/L需要20s,那么再由0.06mol/L降到0.034mol/L所需反应时间应( )
| A. | 等于10s | B. | 等于12s | C. | 小于12s | D. | 大于13s |
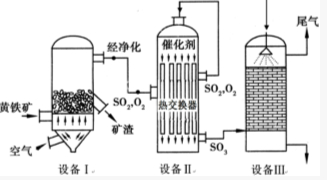 以黄铁矿(主要成分是FeS2)为原料生产硫酸的工艺流程图如下:(1)依据工艺流程图判断下列说法不正确的是(选填序号字母)DF.
以黄铁矿(主要成分是FeS2)为原料生产硫酸的工艺流程图如下:(1)依据工艺流程图判断下列说法不正确的是(选填序号字母)DF.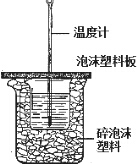 用如图所示装置进行中和热测定实验,请回答下列问题:
用如图所示装置进行中和热测定实验,请回答下列问题: