题目内容
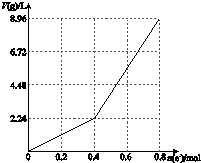
以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体体积V(g)(标准状况)的关系如图所示.下列说法中,正确的是( )
| A.电解前CuSO4溶液的物质的量浓度为2mol/L |
| B.电解后所得溶液中c(H+)=2mol/L |
| C.当n(e-)=0.6mol时,V(H2):V(O2)=2:3 |
| D.向电解后的溶液中加入16gCuO,则溶液可恢复为电解前的浓度 |

A.由生成2.24L气体时转移04mol电子发生2CuSO4+2H2O
2Cu+O2↑+2H2SO4,则n(CuSO4)=
×2=0.2mol,c=
=1mol/L,故A错误;
B.当转移0.4mol电子时,生成n(H2SO4)=0.2mol,c(H+)=
=2mol/L,随电解的进行,水继续电解,溶剂减小,则电解后所得溶液中c(H+)>2mol/L,故B错误;
C.当n(e-)=0.6mol时,发生2CuSO4+2H2O
2Cu+O2↑+2H2SO4、2H2O
2H2↑+O2↑~4e-,n(H2)=
=0.1mol,n(O2)=0.1mol+0.05mol=0.15mol,所以V(H2):V(O2)=0.1mol:0.15mol=2:3,故C正确;
D.因电解后从溶液中析出Cu、氧气、水,则加入16gCuO不会恢复为电解前的浓度,故D错误;
故选C.
| ||
| 2.24L |
| 22.4L/mol |
| 0.2mol |
| 0.2L |
B.当转移0.4mol电子时,生成n(H2SO4)=0.2mol,c(H+)=
| 0.2mol×2 |
| 0.2L |
C.当n(e-)=0.6mol时,发生2CuSO4+2H2O
| ||
| ||
| 0.2mol×2 |
| 4 |
D.因电解后从溶液中析出Cu、氧气、水,则加入16gCuO不会恢复为电解前的浓度,故D错误;
故选C.

练习册系列答案
相关题目



