题目内容
下列各组离子在指定条件下,一定能大量共存的是( )
| A、pH为1的无色溶液:K+、Fe2+、SO32-、Cl- |
| B、能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、Br- |
| C、水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、NO3-、Cl- |
| D、加入铝条有氢气放出的溶液:Na+、NH4+、HCO3-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:A.pH为1的显酸性,Fe2+为浅绿色;
B.能使碘化钾淀粉试纸变蓝的溶液,含氧化性物质;
C.水电离出的c(H+)=1.0×10-12mol?L-1的溶液中,为酸或碱溶液;
D.加入Al能放出H2的溶液,为非氧化性酸或强碱溶液.
B.能使碘化钾淀粉试纸变蓝的溶液,含氧化性物质;
C.水电离出的c(H+)=1.0×10-12mol?L-1的溶液中,为酸或碱溶液;
D.加入Al能放出H2的溶液,为非氧化性酸或强碱溶液.
解答:
解:A.pH为1的显酸性,Fe2+为浅绿色,与无色不符,且Fe2+、SO32-发生相互促进水解反应,不能共存,故A错误;
B.能使碘化钾淀粉试纸变蓝的溶液,含氧化性物质,与S2-发生氧化还原反应,不能共存,故B错误;
C.水电离出的c(H+)=1.0×10-12mol?L-1的溶液中,该组离子之间均不反应,可大量共存,故C正确;
D.加入Al能放出H2的溶液,为非氧化性酸或强碱溶液,碱性溶液中不能存在NH4+、HCO3-,酸溶液中不能大量存在HCO3-,故D错误;
故选C.
B.能使碘化钾淀粉试纸变蓝的溶液,含氧化性物质,与S2-发生氧化还原反应,不能共存,故B错误;
C.水电离出的c(H+)=1.0×10-12mol?L-1的溶液中,该组离子之间均不反应,可大量共存,故C正确;
D.加入Al能放出H2的溶液,为非氧化性酸或强碱溶液,碱性溶液中不能存在NH4+、HCO3-,酸溶液中不能大量存在HCO3-,故D错误;
故选C.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重水解反应、氧化还原反应、复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
关于下列各图的叙述错误的是 ( )


| A、已知1molCO燃烧放出的热为283kJ,2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol则图甲表示CO和H2O(g)生成CO2和H2的能量变化 | ||
| B、常温下0.4 mol?L-1 HB溶液和0.2 mol?L-1NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(B-)>c(Na+)>c(H+)>c(OH-) | ||
| C、常温下,X2(g)和H2反应生成HX的平衡常数如表乙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐渐减小,且HX的还原性逐渐减弱 | ||
D、图丙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,
|
下列说法中错误的是( )
| A、金属晶体的四种堆积模型中,六方最密堆积和面心立方最密堆积的空间利用率最高 |
| B、通过手性合成的方法,可以只得到一种或者主要只得到一种手性分子 |
| C、金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 |
| D、分子形成氢键一定使物质的熔沸点升高 |
医疗上颇为流行的“理疗特效热”,就是利用铁缓慢氧化放出均匀.稳定的热,使患者患处保持温热状态.若1mol铁粉完全氧化成氧化铁,需消耗氧气的质量为( )
| A、24g |
| B、32 g |
| C、21 g |
| D、16 g |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、0.2mol铁粉与足量水蒸气反应生成的H2分子数为0.3NA |
| B、常温常压下,0.1mol Na2O2与CO2完全反应,转移电子数为0.1NA |
| C、50mL18.4mol?L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
| D、某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA |
2003年诺贝尔化学奖授予因发现细胞膜水通道以及对离子通道结构和机理研究作出开创性贡献的两位美国化学家.他们之所以获得化学奖而不是生理或医学奖,目前最合理的解释是( )
| A、该研究与物质有关 |
| B、该研究深入到微观层次 |
| C、该研究深入到分子、原子层次 |
| D、该研究与结构和机理有关 |
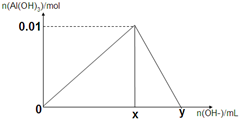 将3mol/L NaOH溶液滴入到25mL一定浓度的AlCl3溶液中.如图是整个过程的数学分析曲线.其中横轴表示加入OH-的体积,纵轴表示产生的Al(OH)3沉淀物质的量.据图示回答下列问题:
将3mol/L NaOH溶液滴入到25mL一定浓度的AlCl3溶液中.如图是整个过程的数学分析曲线.其中横轴表示加入OH-的体积,纵轴表示产生的Al(OH)3沉淀物质的量.据图示回答下列问题: