题目内容
15.晶体是一类非常重要的材料,在很多领域都有广泛的应用.我国现已能够拉制出直径为300毫米,重量达81千克的大直径硅单晶,晶体硅大量用于电子产业.下列对晶体硅的叙述正确的是( )| A. | 晶体硅没有固定的熔沸点 | |
| B. | 形成晶体硅的速率越快越好 | |
| C. | 可用于X-射线衍射实验来鉴别晶体硅和玻璃 | |
| D. | 晶体硅的形成与晶体的自范性有关,形成的晶体无各向异性 |
分析 A.晶体和非晶体的区别:晶体有固定的熔点,非晶体没有固定的熔点;
B.结晶速率太快可能导致晶体质量下降;
C.X射线衍射实验能够测出物质的内部结构,根据微粒是否有规则的排列就能区分出晶体与非晶体;
D.晶体具有各向异性;
解答 解:A.晶体有固定的熔点,非晶体没有固定的熔点,故A错误;
B.晶体的形成都要有一定的形成条件,如温度、压强、结晶速率等,但并不是说结晶速率越快越好,速率太快可能导致晶体质量下降,故B错误;
C.晶体与非晶体最本质的区别是组成物质的粒子在微观空间是否有序排列,x射线衍射可以看到微观结构,所以区别晶体与非晶体最可靠的科学方法是对固体进行x-射线衍射实验,故C正确;
D.晶体硅的形成与晶体的自范性有关,形成的晶体有各向异性,故D错误;
故选C.
点评 本题考查了晶体与非晶体的区别,题目比较简单,注意晶体的结构特点和物理性质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.短周期元素X、Y、M、N的原子序数依次递增,它们的核电荷数之和为32,原子最外层电子数之和为10.X与M同主族,Y与N同主族,X、M原子的最外层电子数之和等于Y原子的次外层电子数.则下列叙述正确的是( )
| A. | 在Y、N的最高价氧化物中,Y、N与氧原子之间均为双键 | |
| B. | 一定条件下,Y单质能置换出N单质,M能置换出X单质 | |
| C. | N元素位于元素周期表中第3周期I V族 | |
| D. | 四种元素的原子半径:X<Y<M<N |
6.某化合物有碳、氢、氧三种元素组成,其红外光谱图有C-H键、O-H键、C-O键的振动吸收,核磁共振氢谱显示该分子中有4个吸收锋,则该有机物的结构简式是( )
| A. | CH3CH(OH)CH3 | B. | CH3CH2CH2CH2OH | C. | CH3CH2CH2OH | D. | CH3CH2OCH2CH3 |
3.某微粒的核外电子排布式为1s22s22p6,下列说法不正确的是( )
| A. | 可以确定该微粒为Ne | |
| B. | 对应元素的单质可能是强还原剂 | |
| C. | 对应元素可能是电负性最大的元素 | |
| D. | 对应元素可能位于元素周期表中第13列 |
10.下列有关σ键和π键的说法错误的是( )
| A. | σ键的特征是轴对称,π键的特征是镜面对称 | |
| B. | 气体单质中一定有σ键,可能有π键 | |
| C. | 乙烯与氢气发生加成反应时,乙烯分子中有π键断裂 | |
| D. | 当原子形成分子时,首先形成σ键,可能形成π键 |
20.卤族元素的单质和化合物很多,我们可以利用所学《物质结构与性质》的相关知识去认识和理解它们.
(1)卤族元素都位于元素周期表的p区(填“s”、“p”、“d”或“ds”).
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是氢键.
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘(写元素名称).
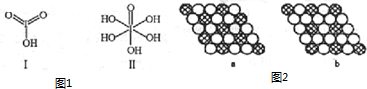
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图1中Ⅰ、Ⅱ所示:
请比较二者酸性的强弱:HIO3>H5IO6(填“>”、“<”或“=”).
(5)如图2所示的二维平面晶体示意图中表示化学式为AX3的是b.(填字母)
(1)卤族元素都位于元素周期表的p区(填“s”、“p”、“d”或“ds”).
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是氢键.
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘(写元素名称).
| 卤族元素 | 氟 | 氯 | 溴 | 碘 |
| 第一电离能(kJ•mol-1) | 1681 | 1251 | 1140 | 1008 |

(4)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图1中Ⅰ、Ⅱ所示:
请比较二者酸性的强弱:HIO3>H5IO6(填“>”、“<”或“=”).
(5)如图2所示的二维平面晶体示意图中表示化学式为AX3的是b.(填字母)
7.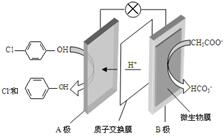 现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚,其原理如图所示,下列说法正确的是( )
现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚,其原理如图所示,下列说法正确的是( )
 现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚,其原理如图所示,下列说法正确的是( )
现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚,其原理如图所示,下列说法正确的是( )| A. | 电流方向从B极沿导线经小灯泡流向A极 | |
| B. | A极的电极反应式为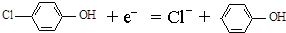 | |
| C. | 当外电路中有0.2mole-转移时,通过质子交换膜的H+的个数为0.2NA | |
| D. | B极为电池的正极,发生还原反应 |
4.配制100mL 0.01mol•L-1KOH溶液时,必须用到的仪器是( )
| A. |  100mL容量瓶 100mL容量瓶 | B. |  100mL集气瓶 | C. |  100mL烧瓶 | D. |  100mL滴瓶 100mL滴瓶 |
5.饱和二氧化硫水溶液中存在下列平衡体系:
SO2+H2O?H++HSO3-
HSO3-?H++SO3-
若向此溶液中( )
SO2+H2O?H++HSO3-
HSO3-?H++SO3-
若向此溶液中( )
| A. | 加水,SO3-浓度增大 | |
| B. | 通入少量Cl2气体,溶液pH增大 | |
| C. | 加少量CaSO3粉末,HSO3-浓度基本不变 | |
| D. | 通入少量HCl气体,溶液中HSO3-浓度减小 |