题目内容
下列有关物质的用途的叙述正确的是( )
| A、可用铝制容器盛装稀硫酸 |
| B、Na2O2可用于呼吸面具中作为氧气的来源 |
| C、FeO常用于制造红色油漆和涂料 |
| D、SiO2可用于制造太阳能电池 |
考点:铝的化学性质,硅和二氧化硅,钠的重要化合物,铁的氧化物和氢氧化物
专题:碳族元素,几种重要的金属及其化合物
分析:A.Al与稀硫酸可持续反应;
B.过氧化钠与二氧化碳反应生成氧气;
C.FeO为黑色固体;
D.Si可用于制造太阳能电池.
B.过氧化钠与二氧化碳反应生成氧气;
C.FeO为黑色固体;
D.Si可用于制造太阳能电池.
解答:
解:A.Al与稀硫酸可持续反应,则不能用铝制容器盛装稀硫酸,但可用铝制容器盛装浓硫酸,故A错误;
B.过氧化钠与二氧化碳反应生成氧气,则Na2O2可用于呼吸面具中作为氧气的来源,故B正确;
C.FeO为黑色固体,则Fe2O3常用于制造红色油漆和涂料,故C错误;
D.Si可用于制造太阳能电池,SiO2为光纤的材料,故D错误;
故选B.
B.过氧化钠与二氧化碳反应生成氧气,则Na2O2可用于呼吸面具中作为氧气的来源,故B正确;
C.FeO为黑色固体,则Fe2O3常用于制造红色油漆和涂料,故C错误;
D.Si可用于制造太阳能电池,SiO2为光纤的材料,故D错误;
故选B.
点评:本题考查物质的性质,综合考查元素化合物的性质,为高频考点,把握性质与用途的关系为解答的关键,注意选项A中不能发生钝化,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列反应属于非氧化还原反应的是( )
A、Fe2O3+3CO2
| ||||
B、NH4NO3
| ||||
C、2NaHCO3
| ||||
D、Cu2(OH)2CO3
|
电子数相等的微粒叫等电子体,下列微粒组是等电子体的是( )
| A、N2O4和NO2 |
| B、Na+和Cl- |
| C、SO42-和PO43- |
| D、NO和O2 |
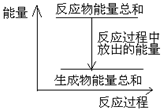 对于敞口容器中的反应:Zn(s)+H2SO4(aq)=ZnSO4 (aq)+H2(g),反应过程中能量关系可用右图表示,下列叙述中不正确的是( )
对于敞口容器中的反应:Zn(s)+H2SO4(aq)=ZnSO4 (aq)+H2(g),反应过程中能量关系可用右图表示,下列叙述中不正确的是( )| A、1 molZn的能量高于1 molH2的能量 |
| B、反应物Zn和H2SO4的总能量高于产物 ZnSO4和H2的总能量 |
| C、如果Zn足量,反应速率会经历由慢到快到慢的过程 |
| D、用锌粉代替锌粒,速率会加快 |
现有pH=a和pH=b的两种NaOH溶液,已知b=a+2,将两种溶液等体积混和后,所得溶液的pH值接近于( )
| A、a-lg2 |
| B、b-lg2 |
| C、a+lg2 |
| D、b+lg2 |
关于化学反应与能量的说法中错误的是( )
| A、中和反应是放出能量的 |
| B、化学反应中有物质变化也有能量变化 |
C、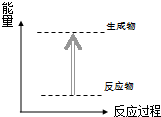 如图所示的反应为放热反应 |
| D、化学键断裂吸收能量,化学键生成放出能量 |
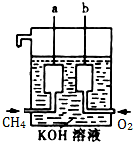 美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:
美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示: