题目内容
13.已知:pOH=-lgc(OH-),298K时,向20.00mL0.10mol•L-1氨水中滴入0.10mol•L-1的盐酸,溶液的pH和pOH与加入盐酸体积关系如图所示.下列说法正确的是( )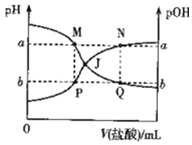
| A. | 曲线PJN表示溶液中pH的变化 | |
| B. | M点水的电离程度比Q点大 | |
| C. | M、P两点的数值之和a+b=14 | |
| D. | pH与pOH交叉点J对应的V(盐酸)=20.00 mL |
分析 pH越大,说明溶液碱性越强,pOH越大,说明溶液酸性越强;
A.根据图知,随着盐酸的加入,氨水溶液中pH减小、pOH增大;
B.酸或碱抑制水电离,含有弱离子的盐促进水电离;
C.根据图知,PJN曲线表示pOH变化、MJQ曲线表示pH变化,M、P点为酸碱中和同一点,M点pH=a、P点pOH=b,则M点c(H+)=10-a mol/L、P点c(OH-)=10-bmol/L,相同温度下c(H+).c(OH-)=Kw;
D.pH与pOH交叉点JpH=pOH,则c(H+)=c(OH-),为中性溶液.
解答 解:pH越大,说明溶液碱性越强,pOH越大,说明溶液酸性越强;
A.根据图知,随着盐酸的加入,氨水溶液中pH减小、pOH增大,所以PJN为溶液中的pOH变化曲线,曲线MJQ表示溶液中pH变化曲线,故A错误;
B.酸或碱抑制水电离,含有弱离子的盐促进水电离,J点为中性溶液,则M点中pH>pOH,溶液呈碱性,Q点溶液呈酸性,M点到J点加入的稀盐酸小于J点到Q点加入的稀盐酸,所以M点溶液中c(OH-)小于Q点溶液中c(H+),则M点水的电离程度比Q点大,故B正确;
C.根据图知,PJN曲线表示pOH变化、MJQ曲线表示pH变化,M、P点为酸碱中和同一点,M点pH=a、P点pOH=b,则M点c(H+)=10-a mol/L、P点c(OH-)=10-bmol/L,相同温度下c(H+).c(OH-)=Kw,所以M、P两点的数值之和a+b=14,故C正确;
D.pH与pOH交叉点JpH=pOH,则c(H+)=c(OH-),为中性溶液,一水合氨是弱碱,要使混合溶液呈中性,则氨水应该稍微过量,所以盐酸体积小于20mL,故D错误;
故选BC.
点评 本题考查酸碱混合溶液定性判断,为高频考点,侧重考查学生图象分析及判断能力,明确溶液中溶质成分及其性质、水电离影响因素是解本题关键,注意:M和P、N和Q点分别是酸碱中和的同一点,为易错点.

 阅读快车系列答案
阅读快车系列答案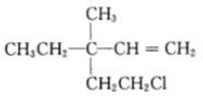 具有手性碳原子,经下面的变化后仍一定具有手性碳原子的是( )
具有手性碳原子,经下面的变化后仍一定具有手性碳原子的是( )| A. | 加成反应 | B. | 消去反应 | C. | 氯代反应 | D. | 水解反应 |
| A. | 离子半径:Rn+>Zm- | |
| B. | 若Y的最高价氧化物对应的水化物HnY0m为强酸,则X的氢化物沸点一定比Y的氢化物的沸点低 | |
| C. | 若X的气态氢化物能使湿润的石蕊试纸变蓝,则标准状况下,18g Y的氢化物的体积为2.24 L | |
| D. | 若R(OH)n为弱电解质,则W(OH)n+1可与KOH溶液反应 |
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 分子中只有共价键的化合物一定是共价化合物 | |
| C. | 离子化合物中只能含离子键 | |
| D. | 只有非金属原子间才能形成共价键 |
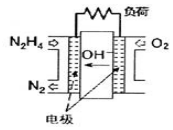 肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )
肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )| A. | 该电池放电时,通入肼的一极为负极 | |
| B. | 电池每释放1mol N2转移的电子数为4NA | |
| C. | 通入空气的一极的电极反应式是:O2+4e-+4H+=2H2O | |
| D. | 电池工作一段时间后,电解质溶液的pH将减小 |
| A. | CaCl2 | B. | CH3COONa | C. | NH3 | D. | Na2S |
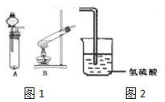 某研究性学习小组设计了一组实验来验证元素周期律.
某研究性学习小组设计了一组实验来验证元素周期律.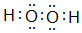 ;
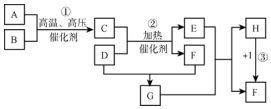
;
 .
.