��Ŀ����
2���Ӵ��������Ṥ���У�������Ӧ���ں��ݡ��¶�Ϊ450�沢�д������ڵ������½��У�2SO2��g��+O2��g��?2SO3��g����H=-190kJ/mol
��������������˵��������Ӧ�Ѵ�ƽ�����cd��
a��v��O2�����T2v��SO3���� b��������������ܶȲ���ʱ����仯
c�������������ƽ����Է�����������ʱ����仯 d������������ķ�����������ʱ����仯
����һ���̶��ݻ�Ϊ5L���ܱ������г���0.20molSO2��0.10molO2������Ӻ�ﵽƽ�⣬��������к�SO30.18mol����v��O2��=0.036mol•L-1•min-1��������ͨ��0.40mol SO2��0.20molO2��ƽ��������Ӧ���� �ƶ����������Ӧ���������淴Ӧ�����������ٴδﵽƽ���0.54mol��n��SO3����0.60mol��
���� �ٸ��ݻ�ѧƽ��״̬�ı�־������Ӧ���ʵ����淴Ӧ���ʣ�ƽ�������и���ɳɷֵĺ����������жϣ�
�ڻ�ѧ��Ӧ���ʵĶ���������������ʣ�����Ӱ�컯ѧƽ����������ж�ƽ���ƶ��������ü�������ٴδ�ƽ���n��SO3���ķ�Χ��
��� �⣺��a���ԣ�O2����=2�ԣ�SO3����������֮�Ȳ����ڻ�ѧ������֮�ȣ��ʴ���
b������������������ܶ�һֱ����ʱ����仯��˵����Ӧ��һ����ƽ��״̬���ʴ���
c���������������Է�����������ʱ����仯��˵����������ʵ����ʵ������䣬��Ӧ��ƽ��״̬������ȷ��
d������������ķ�����������ʱ����仯��˵����������ʵ������䷴Ӧ��ƽ��״̬������ȷ��
��ѡ��cd��
�ڵ�����0.18molSO3ʱ���μӷ�Ӧ�����������ʵ���Ϊx��
2SO2��g��+O2��g��?2SO3��g��
1 2
x 0.18mol
x=$\frac{0.18mol��1}{2}$=0.09mol
v��O2��=$\frac{\frac{0.09mol}{5L}}{0.5min}$=0.036mol��L-1•min-1��
����ͨ��0.40mol SO2��0.20mol O2��������ѹǿ����ƽ�������������С�ķ����ƶ�����������Ӧ�����ƶ���
�ü������n��SO3���ķ�Χ��
����ƽ�ⲻ�ƶ�����ʱn��SO3��=0.18��3=0.54mol��
�����ʱ�ܵ�0.60molSO2��ȫ����SO3�����ݷ�Ӧ����ʽ2SO2��g��+O2��g��?2SO3��g����֪��n��SO3��=0.6mol��
�����ٴδﵽƽ��ʱ��0.54mol��n��SO3����0.60mol��
�ʴ�Ϊ��0.036��������Ӧ����0.54��0.60��
���� ���⿼���˻�ѧƽ��ļ��㡢��ѧƽ���Ӱ�����ؼ���ѧƽ��״̬���жϵ�֪ʶ����Ŀ�Ѷ��еȣ�ע�����ջ�ѧƽ�⼰��Ӱ�����أ���ȷ��ѧ��Ӧ���ʵĸ�����㷽��������������ѧ���ķ�����������������ѧ����������

 ��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�| A�� | �����������Ӧ�Ͻ��̻� | |
| B�� | NH3й¶ʱ���������ˮ�� | |
| C�� | ��Cl2��β���ü���Һ���������ŷ� | |
| D�� | ������ʧ��ʱӦ�����ô�����ˮ���� |
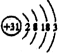 �����й�ϵ����ȷ���ǣ�������
�����й�ϵ����ȷ���ǣ�������| A�� | ԭ�Ӱ뾶��K��Ga��Al | B�� | ���ԣ�KOH��Ga��OH��3��Al��OH�� 3 | ||
| C�� | ���ӵ������ԣ�K+��Ga3+��Al3+ | D�� | ��ˮ��Ӧ�ľ��ҳ̶ȣ�K��Ga��Al |
�ٽ����黻Ϊ�����������ۣ�
�ڼ�������NaNO3���壻
�ۼ�������CuSO4���壻
�ܼ�������CH3COONa���壻
�ݼ��ȣ�
��ϡ���ỻ��98%���ᣬ
���п�����λʱ���������ռ����Ĵ�ʩ�У�������
| A�� | �٢ۢ� | B�� | �٢ۢ� | C�� | �ڢܢ� | D�� | �ڢݢ� |
| ����һ | ������ | |
| A | ���ۺ���ά�ػ�Ϊͬ���칹�� | ���������������Ϊͬϵ�� |
| B | ���ʯ��ʯī��Ϊͬ�������� | O2��O3��Ϊͬλ�� |
| C | SO2��NO2�����ڴ�����Ⱦ�� | pHС��7����ˮ���������� |
| D | ����Ӧ���С���淴Ӧ��ܵķ�Ӧ���ڷ��ȷ�Ӧ | ��Ӧ�������ܺʹ��������������ܺ͵ķ�Ӧ���ڷ��ȷ�Ӧ |
| A�� | A | B�� | B | C�� | C | D�� | D |
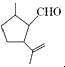 �����м���X�мȺ�̼̼˫���ֺ�ȩ�����Լ���˳����ȷ���ǣ�������
�����м���X�мȺ�̼̼˫���ֺ�ȩ�����Լ���˳����ȷ���ǣ�������| A�� | �ȼ����Ը��������Һ�����������Һ������ | |
| B�� | �ȼ���ˮ��������Ը��������Һ | |
| C�� | �ȼ�������Һ�����ȣ��ټ�����ˮ | |
| D�� | �ȼ�������������ͭ����Һ�����ȣ�ȡ��Һ�ữ���ټ���ˮ |
| A�� | 0.5mol C4H10�к��еĹ��ۼ���Ϊ6.5NA | |
| B�� | 3.4 g�ǻ���3.4 g������������2NA������ | |
| C�� | 1L0.1 mol•L-1CH3COOH��Һ�к��е���ԭ����Ϊ0.2NA | |
| D�� | ��״���£�22.4L��CHCl3��CH2Cl2��ɵĻ�����к��еķ�����ĿΪNA |