��Ŀ����
 ���Ȼ�������ѧ��ѧʵ�����в���ȱ�ٵ���Ҫ�Լ���
���Ȼ�������ѧ��ѧʵ�����в���ȱ�ٵ���Ҫ�Լ���ijͬѧ���÷���м��������ͭ�Ȳ������ᷴӦ�����ʣ����Ʊ�FeCl3?6H2O����ͬѧ��Ƶ�ʵ��װ����ͼ��ʾ��A�з��з���м���ձ���ʢ�й�����ϡ���ᣬʵ��ʱ��a���ر�b���ӷ�Һ©������A�еμӹ������ᣬ��ʱ��Һ��dz��ɫ���ٴ�b���й��ˣ����˽�����ȡ�ձ�����Һ�����������м��ȣ�����������ˮ����ȥ�����HNO3���ٽ��½ᾧ��FeCl2?6H2O���壬��д���пհף�
��1���μ�����ʱ�����ַ�Ӧ���ʱ������봿���۵ķ�Ӧ�죬��ԭ����
��2���ձ���ϡHNO3�������ǣ������ӷ���ʽ��ʾ��
��3������ʵ������У����ɼ�a����ʼ�մ���Ŀ����
��4�������ý��½ᾧ�ķ�����ȡFeCl3?6H2O������ֱ�ӽ���Һ������������ų������յõ��Ĺ�����
���㣺ʵ��װ���ۺ�,���Ļ�ѧ����,�Ʊ�ʵ�鷽�������
ר�⣺ʵ����
��������1���γ�ԭ���ʹ��Ӧ���ʼӿ죻
��2��ϡHNO3��ǿ�����ԣ�ʹFe2+ ȫ��������Fe3+��
��3���������ͨ��ʹ��Һ©���е���ɵ���A�У�
��4���Ȼ�����ˮ����������������
��2��ϡHNO3��ǿ�����ԣ�ʹFe2+ ȫ��������Fe3+��
��3���������ͨ��ʹ��Һ©���е���ɵ���A�У�
��4���Ȼ�����ˮ����������������
���
�⣺��1������м��������ͭ���ʣ��������Cu�����γ�Fe-Cuԭ���ʹ��Ӧ���ʼӿ죬
�ʴ�Ϊ������м�еIJ�����������Fe�������й���ԭ��أ��ӿ��˷�Ӧ���ʣ�
��2��������ϡHNO3��֤ʹFe2+ ȫ��������Fe3+����Ӧ�����ӷ���ʽ��3Fe2++4H++NO3-�T3Fe3++NO��+2H2O��
�ʴ�Ϊ��3Fe2++4H++NO3-�T3Fe3++NO��+2H2O��
��3������ʵ������У����ɼ�a���������װ���������ͬ��ʹ��Һ©���е���ɵ���A�У�
�ʴ�Ϊ��ʹװ���ڲ�����������ͨ������A��Һ�����£�
��4���Ȼ�������ǿ����������ˮ�⣬���ȴٽ�ˮ�⣬����FeCl3+3H2O?Fe��OH��3+3HCl������Fe��OH��3�����ᣬ����ӷ�����Һ�д��ڴ�����Fe��OH��3��
�ʴ�Ϊ��Fe��OH��3��
�ʴ�Ϊ������м�еIJ�����������Fe�������й���ԭ��أ��ӿ��˷�Ӧ���ʣ�
��2��������ϡHNO3��֤ʹFe2+ ȫ��������Fe3+����Ӧ�����ӷ���ʽ��3Fe2++4H++NO3-�T3Fe3++NO��+2H2O��
�ʴ�Ϊ��3Fe2++4H++NO3-�T3Fe3++NO��+2H2O��
��3������ʵ������У����ɼ�a���������װ���������ͬ��ʹ��Һ©���е���ɵ���A�У�
�ʴ�Ϊ��ʹװ���ڲ�����������ͨ������A��Һ�����£�
��4���Ȼ�������ǿ����������ˮ�⣬���ȴٽ�ˮ�⣬����FeCl3+3H2O?Fe��OH��3+3HCl������Fe��OH��3�����ᣬ����ӷ�����Һ�д��ڴ�����Fe��OH��3��
�ʴ�Ϊ��Fe��OH��3��
���������⿼�������仯���������ʵ�飬Ϊ��Ƶ���㣬����ѧ���ķ���������ʵ�������Ŀ��飬ע����ΪFeCl3��ǿ��������ˮ�⣺FeCl3+3H2O?Fe��OH��3+3HCl����������ʱʹHCl�ӷ����ˮ��ƽ�����ƣ���˵ò���FeCl3?6H2O���ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
��֪Ԫ�ص�ԭ����������������֪ԭ�ӵ���������У�������
| A�������� |
| B���˵���� |
| C����������� |
| D�������ڱ��е�λ�� |
��0.1mol/L Na2CO3��Һ�У�������֮��������й�ϵ�����в���ȷ���ǣ�������
| A��c��Na+��+c��H+��=2c��CO32-��+c��HCO3-��+c��OH-�� |
| B��c��Na+��={c��CO32-��+c��HCO3-��+c��H2CO3��} |
| C��c��OH-��=c��H+��+c��HCO3-��+2c��H2CO3�� |
| D��c��Na+����c��HCO3-����c��OH-����c��H+�� |
���������ܷ�����ȥ��Ӧ���ǣ�������
| A����������NaOH����Һ���� |
| B��һ�ȼ�����NaOH����Һ���� |
| C����������NaOHˮ��Һ���� |
| D���Ҵ���Ũ���Ṳ����170�� |


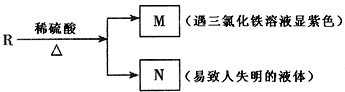
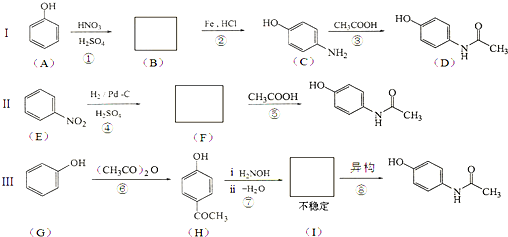
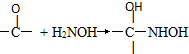
 ��
�� ��
��