题目内容
将5.6gFe加入到100mL的稀硫酸中溶液中,恰好完全反应.
(1)写出该反应的化学方程式,并标出电子转移方向和数目.
(2)试求生成气体在标准状况下的体积和稀硫酸的物质的量浓度.
(3)计算反应中转移的电子.
(1)写出该反应的化学方程式,并标出电子转移方向和数目.
(2)试求生成气体在标准状况下的体积和稀硫酸的物质的量浓度.
(3)计算反应中转移的电子.
考点:氧化还原反应的电子转移数目计算
专题:氧化还原反应专题
分析:(1)铁与稀硫酸反应生成硫酸亚铁和氢气,分析反应中各元素化合价变化分析氧化还原反应,标出电子转移方向和数目;
(2)依据方程式计算生成氢气的物质的量,然后转化为标况下体积;计算消耗的硫酸的物质的量,依据C=
计算硫酸的物质的量浓度;
(3)依据方程式计算转移的电子数目.
(2)依据方程式计算生成氢气的物质的量,然后转化为标况下体积;计算消耗的硫酸的物质的量,依据C=
| n |
| V |
(3)依据方程式计算转移的电子数目.
解答:
解:Fe的物质的量为
=0.1mol,
(1)铁与稀硫酸反应生成硫酸亚铁和氢气,方程式为:Fe+H2SO4═FeSO4+H2↑,反应中1mol铁失去2mol电子转化成1mol二价铁离子,2mol氢离子得到2mol电子生成1mol氢气,电子转移方向和数目表示为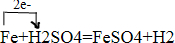 ;
;
答:该反应的化学方程式为Fe+H2SO4═FeSO4+H2↑;电子转移方向和数目为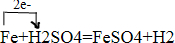 ;
;
(2)由Fe+H2SO4═FeSO4+H2↑可知
Fe+H2SO4═FeSO4+H2↑
1 1 1
0.1mol n(H2SO4) n(H2)
解得:n(H2SO4)=n(H2)=0.1mol;
生成氢气在标准状况下的体积V=0.1mol×22.4L/mol=2.24L;
稀硫酸的物质的量浓度C=
=1mol/L;
答:生成气体在标准状况下的体积为2.24L;稀硫酸的物质的量浓度为1mol/L;
(3)Fe+H2SO4═FeSO4+H2↑,反应中1mol铁失去2mol电子转化成1mol二价铁离子,2mol氢离子得到2mol电子生成1mol氢气,所以0.1mol铁参加反应转移0.2mol电子;
答:反应中转移的电子为0.2mol.
| 5.6g |
| 56g/mol |
(1)铁与稀硫酸反应生成硫酸亚铁和氢气,方程式为:Fe+H2SO4═FeSO4+H2↑,反应中1mol铁失去2mol电子转化成1mol二价铁离子,2mol氢离子得到2mol电子生成1mol氢气,电子转移方向和数目表示为
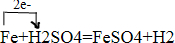 ;
;答:该反应的化学方程式为Fe+H2SO4═FeSO4+H2↑;电子转移方向和数目为
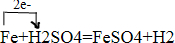 ;
;(2)由Fe+H2SO4═FeSO4+H2↑可知
Fe+H2SO4═FeSO4+H2↑
1 1 1
0.1mol n(H2SO4) n(H2)
解得:n(H2SO4)=n(H2)=0.1mol;
生成氢气在标准状况下的体积V=0.1mol×22.4L/mol=2.24L;
稀硫酸的物质的量浓度C=
| 0.1mol |
| 0.1L |
答:生成气体在标准状况下的体积为2.24L;稀硫酸的物质的量浓度为1mol/L;
(3)Fe+H2SO4═FeSO4+H2↑,反应中1mol铁失去2mol电子转化成1mol二价铁离子,2mol氢离子得到2mol电子生成1mol氢气,所以0.1mol铁参加反应转移0.2mol电子;
答:反应中转移的电子为0.2mol.
点评:本题考查了有关方程式的计算及氧化还原反应分析,明确发生的反应及反应中元素化合价变化是解题关键,题目难度不大.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
保护环境是每一个公民的责任,下列说法正确的是( )
| A、大量使用含磷洗涤剂会带来“白色污染” |
| B、减少并逐渐停止生产和使用氟氯代烷的目的是为了减少酸雨 |
| C、废旧电池中的汞、镉、铅等重金属盐不会对土壤和水源造成污染 |
| D、一个现代化的化工企业,应该朝着无废物排出的“封闭式生产”的方向努力 |
已知Fe3+、Fe2+、NO3-、NH4+、H+和H2O六种微粒属于一个氧化还原反应中的反应物和生成物.下列叙述中不正确的是( )
| A、还原产物为NH4+ |
| B、氧化剂与还原剂的物质的量之比为1:8 |
| C、Fe3+和Fe2+分别属于反应物和生成物 |
| D、若把该反应设计为原电池,则负极反应为Fe2+-e-=Fe3+ |
下列说法正确的是( )
| A、物质发生化学变化都伴随着能量变化 |
| B、任何反应中的能量变化都表现为热量变化 |
| C、伴有能量变化的物质变化都是化学变化 |
| D、没有物质的变化,就没有能量的变化 |
分析下图所示的四个原电池装置,其中结论正确的是( )

| A、①②中Mg作负极,③④中Fe作负极 |
| B、②中Mg作正极,电极反应式为6H2O+6e-═6OH-+3H2↑ |
| C、③中Cu作负极,电极反应式为Cu-2e-═Cu2+ |
| D、④中Cu作正极,电极反应式为2H++2e-═H2↑ |
涂改液是一种使用率较高的文具,经实验证明,涂改液中含有苯的同系物和卤代烃.下列说法中不正确的是( )
| A、涂改液危害人体健康、污染环境 |
| B、中小学生最好不用或慎用涂改液 |
| C、苯的同系物和卤代烃没有刺鼻气味 |
| D、苯的同系物和卤代烃是涂改液中的溶剂 |