题目内容
3.汽车尾气排放的一氧化碳、氮氧化物等气体已成为大气污染的主要来源.德国大众汽车尾气检测造假事件引起全世界震惊.根据下列示意图(如图1)回答有关问题: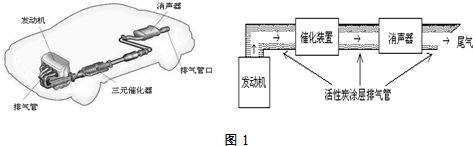
(1)汽车发动机工作时会引发N2(g)+O2(g)=2NO(g)△H=+180kJ•mol-1,其能量变化示意图如下:
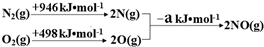
则NO中氮氧键的键能为632kJ•mol-1.
(2)空燃比过小易产生CO.有人提出可以设计反应2CO(g)=2C(s)+O2(g)来消除CO的污染.判断该设想是否可行,并说出理由不合理,该反应焓增、熵减,任何条件下都不能自发进行或该反应△H>0,△S<0则△G>0.
(3)利用活性炭涂层排气管处理NOx的反应为:xC(s)+2NOx(g)?N2(g)+xCO2 (g)△H=-b kJ•mol-1.若使NOx更加有效的转化为无毒尾气排放,以下措施理论上可行的是AD.
A.增加排气管长度 B.增大尾气排放口
C.升高排气管温度 D.添加合适的催化剂
(4)催化装置中涉及的反应之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).
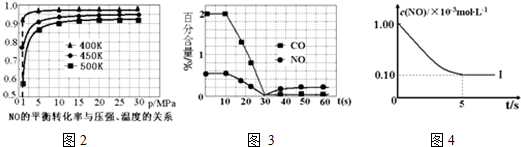
①探究上述反应中NO的平衡转化率与压强、温度的关系,得到图2所示的曲线.催化装置比较适合的温度和压强是400K,1MPa.
②测试某型号汽车在冷启动(冷启动指发动机水温低的情况下启动)时催化装置内CO和NO百分含量随时间变化曲线如图3所示.则前10s 内,CO和NO百分含量没明显变化的原因是尚未达到催化剂工作温度(或尚未达到反应的温度).
③研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了以下三组实验:
| 实验编号 | T(K) | NO初始浓度 (mol•L-1) | CO初始浓度 (mol•L-1) | 催化剂的比表面积(m2/g) |
| Ⅰ | 400 | 1.00×10-3 | 3.60×10-3 | 82 |
| Ⅱ | 400 | 1.00×10-3 | 3.60×10-3 | 124 |
| Ⅲ | 450 | 1.00×10-3 | 3.60×10-3 | 124 |
分析 (1)△H=反应物的键能总和-生成物的键能总和;
(2)根据△H-T△H<0来判断反应的自发性;
(3)A.增加排气管长度,增大了相当于增大了固体的接触面积,加快了化学反应速率,对平衡无影响;
B.增大尾气排放口,对反应速率和平衡不产生影响;
C.升高排气管温度,温度升高,平衡左移,不利于NOx转化;
D.添加合适的催化剂,加快化学反应速率,对平衡无影响;
(4)①综合考虑NO的转化率和成本;
②汽车冷启动时的尾气催化处理CO、NO百分含量随时间变化曲线变化分析,开始的气体含量变化不大,说明温度低,催化剂的作用未起作用;
③结合表格中的浓度,利用三段法列出400K时平衡浓度,带入平衡常数表达式计算;根据外界条件对化学反应速率和化学平衡的影响判断.
解答 解:(1)设NO中氮氧键的键能为x,
△H=反应物的键能总和-生成物的键能总和=(946+498)kJ•mol-1-2×x=180kJ•mol-1,解得x=632 kJ•mol-1,
故答案为:632;
(2)2CO(g)=2C(s)+O2(g)(△H>0、△S<0)是一个焓增、熵减的反应,任何情况下不能自发进行,所以无法消除CO的污染,
故答案为:不合理,该反应焓增、熵减,任何条件下都不能自发进行或该反应△H>0,△S<0则△G>0;
(3)xC(s)+2NOx(g)?N2(g)+xCO2 (g)△H=-b kJ•mol-1.此反应为放热反应,
A.增加排气管长度,增大了相当于增大了固体的接触面积,加快了化学反应速率,故A正确;
B.增大尾气排放口,对反应速率和平衡不产生影响,故B错误;
C.升高排气管温度,温度升高,平衡左移,不利于NOx转化,故C错误;
D.添加合适的催化剂,加快化学反应速率,故D正确;
故答案为:AD;
(4)①由图2可知,等压条件下,温度越低,NO的转化率越高,因此温度选400K,同温下,NO的转化率随着温度的升高变化不大,所以选用较为经济的1MPa,
故答案为:400K,1MPa:
②汽车冷启动时的尾气催化处理CO、NO百分含量随时间变化曲线变化分析,开始的气体含量变化不大,说明温度低,催化剂的作用未起作用;证明反应未达到催化剂工作温度(或尚未达到反应的温度);
故答案为:尚未达到催化剂工作温度(或尚未达到反应的温度);
③设400K达到平衡状态时,则
2NO(g)+2CO(g)?N2(g)+2CO2(g).
初始浓度(10-3mol•L-1):1 3.60 0 0
转化浓度(10-3mol•L-1):0.9 0.9 0.45 0.9
平衡浓度(10-3mol•L-1):0.1 2.7 0.45 0.9
K=$\frac{0.45×1{0}^{-3}mol•{L}^{-1}×(0.9×1{0}^{-3}mol•{L}^{-1})^{2}}{(2.7×1{0}^{-3}mol•{L}^{-1})^{2}×(0.1×1{0}^{-3}mol•{L}^{-1})^{2}}$=5000L•mol-1,
因Ⅰ、Ⅱ温度相同,初始浓度相等,催化剂对平衡移动无影响,则平衡不移动,但Ⅱ的速率大,则Ⅱ先达到化学平衡,Ⅰ、Ⅱ达平衡时NO的浓度相同,而Ⅲ的温度高,则反应速率最大且平衡逆移,即达到化学平衡时c(NO)增大,实验Ⅱ、Ⅲ条件下混合气体中NO浓度随时间变化的趋势曲线图为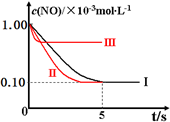 ,
,
故答案为:5000L•mol-1; .
.
点评 本题考查较为综合,涉及反应热的计算、反应自发性的判断、化学反应速率和化学平衡的影响因素与图象的关系、平衡常数的计算等知识,为高频考点,其中(4)③是难点,把握控制变量法分析反应速率的影响因素及图象为解答的关键,题目难度较大.

| A. | A+n+m | B. | A+n-m | C. | A-n+m | D. | A-n-m |
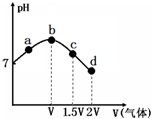 常温常压下,将NH3缓慢通入饱和食盐水中至饱和,然后向所得溶液中缓慢通入CO2,整个实验进程中溶液的pH随通入气体体积的变化曲线如图所示(实验中不考虑氨水的挥发).下列叙述不正确的是( )
常温常压下,将NH3缓慢通入饱和食盐水中至饱和,然后向所得溶液中缓慢通入CO2,整个实验进程中溶液的pH随通入气体体积的变化曲线如图所示(实验中不考虑氨水的挥发).下列叙述不正确的是( )| A. | 由a点到b点的过程中,溶液中$\frac{{c(N{H_3}•{H_2}O)}}{c(NH_4^+)}$增大 | |
| B. | 由图可知(NH4)2CO3溶液显碱性、NH4Cl溶液显酸性 | |
| C. | c点所示溶液中,c(NH4+)>c(CO32-)>c(OH-)>c(H+) | |
| D. | d点所示溶液中,c(NH4+)+c(NH3•H2O)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| A. | 乙炔 | B. | 2-丁炔 | C. | 2-丁烯 | D. | 1,3-丁二烯 |
| A. | NaClO溶液 | B. | 干燥的氯气 | C. | 氯水 | D. | 次氯酸钙溶液 |
| A. | Al2O3$→_{△}^{NaOH(aq)}$NaAlO2$\stackrel{CO_{2}}{→}$Al(OH)3 | |
| B. | Si$→_{△}^{O_{2}}$SiO2$\stackrel{H_{2}O}{→}$H2SiO3 | |
| C. | Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3$\stackrel{△}{→}$无水FeCl3 | |
| D. | MgCl2(aq)$\stackrel{石灰乳}{→}$Mg(OH2)$\stackrel{△}{→}$MgO |
| A. | 碘的升华、溴水中萃取溴、石油的分馏、煤的干馏均是物理变化 | |
| B. | BaSO4难溶于水是弱电解质,在医学上用作钡餐 | |
| C. | 14C可用于文物年代的鉴定,14C与12C互为同位素 | |
| D. | 明矾是常用的净水剂,可以杀菌、消毒 |
 (1)铝热反应在工业生产中的重要用途之一是焊接钢轨或冶炼难熔金属等;用化学方程式表示出其中的原理2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe(举一例).铝制品因为表面易形成致密的氧化铝薄膜而经久耐用,但是该氧化膜易被酸、碱破坏,若将表面有一层氧化铝薄膜的铝条和氢氧化钠溶液作用,反应的化学方程式为Al2O3+2NaOH═2NaAlO2+H2O、2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(1)铝热反应在工业生产中的重要用途之一是焊接钢轨或冶炼难熔金属等;用化学方程式表示出其中的原理2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe(举一例).铝制品因为表面易形成致密的氧化铝薄膜而经久耐用,但是该氧化膜易被酸、碱破坏,若将表面有一层氧化铝薄膜的铝条和氢氧化钠溶液作用,反应的化学方程式为Al2O3+2NaOH═2NaAlO2+H2O、2Al+2NaOH+2H2O=2NaAlO2+3H2↑.