题目内容
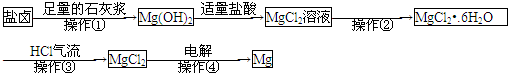
某工厂用提取粗盐后的盐卤(主要成分为MgCl2)制备金属镁,其工艺流程图如下所示.下列说法错误的是( )

| A、若在实验室进行操作①,只需要漏斗和烧杯两种玻璃仪器 |
| B、操作①发生的反应为非氧化还原反应 |
| C、操作②是蒸发浓缩结晶 |
| D、在整个制备过程中,未发生置换反应 |
考点:海水资源及其综合利用,金属冶炼的一般原理
专题:
分析:盐卤加入足量石灰浆沉淀镁离子生成氢氧化镁沉淀,过滤得到沉淀加入适量盐酸溶解得到氯化镁溶液,通过蒸发浓缩结晶得到氯化镁晶体,在氯化氢气流中失水得到固体氯化镁,电解熔融氯化镁得到金属镁;
A.过滤操作中需要使用漏斗和烧杯、玻璃棒;
B.操作①发生的反应为沉淀镁离子的反应,发生的是复分解反应,是非氧化还原反应;
C.操作②是MgCl2溶液得到MgCl2晶体;
D.置换反应中应是单质与化合物反应生成单质和化合物.
A.过滤操作中需要使用漏斗和烧杯、玻璃棒;
B.操作①发生的反应为沉淀镁离子的反应,发生的是复分解反应,是非氧化还原反应;
C.操作②是MgCl2溶液得到MgCl2晶体;
D.置换反应中应是单质与化合物反应生成单质和化合物.
解答:
解:A.过滤操作中需要使用漏斗和烧杯、玻璃棒,故A错误;
B.操作①是沉淀镁离子,发生的是复分解反应,故B正确;
C.MgCl2溶液得到MgCl2晶体需要蒸发浓缩结晶,故C正确;
D.只发生复分解反应、氧化还原反应、分解反应,未发生置换反应,故D正确.
故选A.
B.操作①是沉淀镁离子,发生的是复分解反应,故B正确;
C.MgCl2溶液得到MgCl2晶体需要蒸发浓缩结晶,故C正确;
D.只发生复分解反应、氧化还原反应、分解反应,未发生置换反应,故D正确.
故选A.
点评:本题考查元素及其化合物,明确流程中发生的化学反应是解答的关键,注意基本反应类型的区别,题目难度中等.

练习册系列答案
相关题目
酸雨中存在电离平衡:H2SO3?H++HSO3-、HSO3-?H++SO32-,下列有关说法不正确的是( )
A、常温下,加入蒸馏水稀释酸雨,c(H2SO3)、
| ||
| B、常温下,第一步电离常数K1大于第二步电离常数K2 | ||
| C、不考虑亚硫酸分解和会发,适当升温,平衡向右移动,电离常数增大 | ||
| D、温度不变时,随着酸雨放置时间延长,酸性增强. |
鉴别下列各物质,只能用焰色反应的是( )
| A、NaCl和KCl |
| B、KCl和NaNO3 |
| C、NaCl和CuSO4 |
| D、NaCl和 K2CO3 |
下列反应的离子方程式错误的是( )
| A、磷酸与氢氧化钾溶液反应:H++OH-=H2O |
| B、澄清石灰水跟稀硝酸反应:H++OH-=H2O |
| C、醋酸铵和盐酸反应:CH3COO-+H+=CH3COOH |
| D、碳酸钙溶于硝酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
将AlCl3、FeCl2、FeCl3、MgCl2四种溶液,只用一种试剂就能加以区别,这种试剂是( )
| A、HCl |
| B、NaOH |
| C、BaCl2 |
| D、KSCN |
 由徐光宪院士发起、院士学子同创的《分子共和国》科普读物最近出版了.全书形象生动地戏说了BF3、TiO2、CH3COOH、CO2、NO、二茂铁、NH3、HCN、H2S、O3、异戊二烯和萜等众多“分子共和国”中的明星.
由徐光宪院士发起、院士学子同创的《分子共和国》科普读物最近出版了.全书形象生动地戏说了BF3、TiO2、CH3COOH、CO2、NO、二茂铁、NH3、HCN、H2S、O3、异戊二烯和萜等众多“分子共和国”中的明星.