题目内容
已知多元弱酸在水溶液中的电离是分步进行的,且第一步电离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度…
今有HA、H2B、H3C三种一元、二元、三元弱酸,
根据“较强酸+较弱酸盐=较强酸盐+较弱酸”的反应规律,它们之间能发生下列反应:
①HA+HC2-(少量)=A-+H2C-;
②H2B(少量)+2A-=B2-+2HA;
③H2B(少量)+H2C-=HB-+H3C
回答下列问题:
(1)相同条件下,HA、H2B、H3C三种酸中酸性最强的是 .
(2)A-、B2-、C3-、HB-、H2C-、HC2-六种离子中,最易结合质子(H+)的是 ,最难结合质子的是 .
(3)完成下列反应的离子方程式
④H3C+A-: ;⑤HB-+A-: ;⑥H3C+B2-: .
今有HA、H2B、H3C三种一元、二元、三元弱酸,
根据“较强酸+较弱酸盐=较强酸盐+较弱酸”的反应规律,它们之间能发生下列反应:
①HA+HC2-(少量)=A-+H2C-;
②H2B(少量)+2A-=B2-+2HA;
③H2B(少量)+H2C-=HB-+H3C
回答下列问题:
(1)相同条件下,HA、H2B、H3C三种酸中酸性最强的是
(2)A-、B2-、C3-、HB-、H2C-、HC2-六种离子中,最易结合质子(H+)的是
(3)完成下列反应的离子方程式
④H3C+A-:
考点:弱电解质在水溶液中的电离平衡,离子方程式的书写
专题:离子反应专题,电离平衡与溶液的pH专题
分析:首先,根据题目中的信息,判断酸性顺序:第一步电离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度,得到
H2B>HB-、H3C>H2C->HC2-,它们之间能发生下列反应,得到
①HA+HC2-(少量)=A-+H2C-
即HA>H2C-,同时,即使HA过量,也只能生成H2C-,而不是H3C,说明HA<H3C,
②H2B(少量)+2A-=2HA+B2-
即H2B>HA,同时,由于H2B很少,并生成B2-,即说明H2B将2个H+都给了A-,即HB-也能将H+给A-,
即说明H2B>HB->HA
③H2B(少量)+H2C-=HB-+H3C
即H2B>H3C,但是生成HB-,即说明HB-不能将H+提供,即HB-<H3C,即H2B>H3C>HB-
综合,得到H2B>H3C>HB->HA>H2C->HC2-
然后利用这个顺序进行判断.
H2B>HB-、H3C>H2C->HC2-,它们之间能发生下列反应,得到
①HA+HC2-(少量)=A-+H2C-
即HA>H2C-,同时,即使HA过量,也只能生成H2C-,而不是H3C,说明HA<H3C,
②H2B(少量)+2A-=2HA+B2-
即H2B>HA,同时,由于H2B很少,并生成B2-,即说明H2B将2个H+都给了A-,即HB-也能将H+给A-,
即说明H2B>HB->HA
③H2B(少量)+H2C-=HB-+H3C
即H2B>H3C,但是生成HB-,即说明HB-不能将H+提供,即HB-<H3C,即H2B>H3C>HB-
综合,得到H2B>H3C>HB->HA>H2C->HC2-
然后利用这个顺序进行判断.
解答:
解:(1)根据题目中的信息,判断酸性顺序:第一步电离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度,得到
H2B>HB-H3C>H2C->HC2-它们之间能发生下列反应,
①HA+HC2-(少量)=A-+H2C-,即HA>H2C-,同时,即使HA过量,也只能生成H2C-,而不是H3C,说明HA<H3C,
②H2B(少量)+2A-=2HA+B2-,即H2B>HA,同时,由于H2B很少,并生成B2-,即说明H2B将2个H+都给了A-,即HB-也能将H+给A-,
即说明H2B>HB->HA,
③H2B(少量)+H2C-=HB-+H3C,
即H2B>H3C,但是生成HB-,即说明HB-不能将H+提供,即HB-<H3C,即H2B>H3C>HB-,
综合信息得到H2B>H3C>HB->HA>H2C->HC2-,所以最强的酸为H2B,故答案为:H2B;
(2)由以上酸性强弱顺序知:物质的酸性越强,其对应酸根离子结合质子的能力越弱,反之越强,所以最易结合质子的是C3-,最难结合质子的是HB-.
故答案为:C3-;HB-;
(3)根据H2B>H3C>HB->HA>H2C->HC2-,以及强酸制弱酸的原则,故离子方程式为:④H3C+A-=HA+H2C-;⑤HB-+A-=HA+B-;⑥H3C+B2-=HB-+H2C-
故答案为:④H3C+A-=HA+H2C-;⑤HB-+A-=HA+B-;⑥H3C+B2-=HB-+H2C-
H2B>HB-H3C>H2C->HC2-它们之间能发生下列反应,
①HA+HC2-(少量)=A-+H2C-,即HA>H2C-,同时,即使HA过量,也只能生成H2C-,而不是H3C,说明HA<H3C,
②H2B(少量)+2A-=2HA+B2-,即H2B>HA,同时,由于H2B很少,并生成B2-,即说明H2B将2个H+都给了A-,即HB-也能将H+给A-,
即说明H2B>HB->HA,
③H2B(少量)+H2C-=HB-+H3C,
即H2B>H3C,但是生成HB-,即说明HB-不能将H+提供,即HB-<H3C,即H2B>H3C>HB-,
综合信息得到H2B>H3C>HB->HA>H2C->HC2-,所以最强的酸为H2B,故答案为:H2B;
(2)由以上酸性强弱顺序知:物质的酸性越强,其对应酸根离子结合质子的能力越弱,反之越强,所以最易结合质子的是C3-,最难结合质子的是HB-.
故答案为:C3-;HB-;
(3)根据H2B>H3C>HB->HA>H2C->HC2-,以及强酸制弱酸的原则,故离子方程式为:④H3C+A-=HA+H2C-;⑤HB-+A-=HA+B-;⑥H3C+B2-=HB-+H2C-
故答案为:④H3C+A-=HA+H2C-;⑤HB-+A-=HA+B-;⑥H3C+B2-=HB-+H2C-
点评:本题综合考查弱电解质的电离问题,题目较难,做题时注意把握“较强酸+较弱酸盐→较强酸盐+较弱酸”的反应规律.

练习册系列答案
相关题目
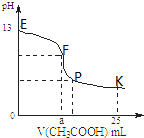 25℃时,在25mL0.1mol/L的NaOH溶液中逐渐滴加入0.2mol/L CH3COOH溶液,混合溶液pH的变化曲线如图所示,下列分析结论不正确的是( )
25℃时,在25mL0.1mol/L的NaOH溶液中逐渐滴加入0.2mol/L CH3COOH溶液,混合溶液pH的变化曲线如图所示,下列分析结论不正确的是( )| A、a=12.5,且混合溶液pH=7 |
| B、对应曲线上E、F间任何一点,溶液中都有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| C、P点时,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D、K点时,c(CH3COO-)+c(CH3COOH)=2c(Na+) |
某温度下,已知反应mX(g)+nY(g)?qZ(g)△H>0,m+n>q,在体积一定的密闭容器中投入反应物达到平衡,下列叙述正确的是( )
| A、通惰性气体增大压强,平衡正向移动 | ||
| B、再加入X,反应吸收的热量增大 | ||
| C、增加Y的物质的量,X的转化率减小 | ||
D、降低温度,
|
下列反应是工业生产硝酸的一个反应过程,4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-1025kJ/mol,若反应物起始的物质的量相同.下列关于该反应的示意图不正确的是( )
A、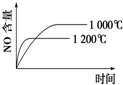 |
B、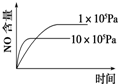 |
C、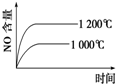 |
D、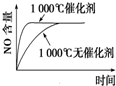 |
在一定条件下,可发生反应:RO3n-+F2+2OH-═RO4-+2F-+H2O.则RO3n-中R元素的化合价是( )
| A、+4 | B、+5 | C、+6 | D、+7 |
硬铝的主要成分是( )
| A、纯铝 | B、钢化玻璃 |
| C、沙子 | D、镁铝合金 |