题目内容
7.已知下列反应的热化学方程式:?6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1
?2H2(g)+O2(g)═2H2O(g)△H2
?C(s)+O2(g)═CO2(g)△H3
则反应12CO2(g)+10H2O(g)+O2(g)+6N2(g)═4C3H5(ONO2)3(l)的△H为( )
| A. | 12△H3+5△H2-2△H1 | B. | 2△H1-5△H2-12△H3 | C. | 12△H3-5△H2-2△H1 | D. | △H1-5△H2-12△H3 |
分析 已知:①.?6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1
②.?2H2(g)+O2(g)═2H2O(g)△H2
③.?C(s)+O2(g)═CO2(g)△H3
根据盖斯定律,①×2-②×5-③×12可得:12CO2(g)+10H2O(g)+O2(g)+6N2(g)═4C3H5(ONO2)3(l),反应热也进行相应计算.
解答 解:已知:①.?6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1
②.?2H2(g)+O2(g)═2H2O(g)△H2
③.?C(s)+O2(g)═CO2(g)△H3
根据盖斯定律,①×2-②×5-③×12可得:12CO2(g)+10H2O(g)+O2(g)+6N2(g)═4C3H5(ONO2)3(l),则△H=2△H1-5△H2-12△H3,
故选:B.
点评 本题考查运用盖斯定律计算反应热,关键是根据已知热化学方程式构造目标热化学方程式,注意对盖斯定律理解与应用.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
2.如图装置中,溶液体积均为200ml,开始时,电解质溶液的浓度均为0.1mol•L-1,工作一段时间后,测得导线上通过了0.02mol电子,若不考虑溶液体积的变化,下列叙述中正确的是( )
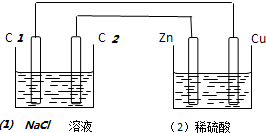

| A. | (1)中C2电极反应式为:2Cl--2e-═Cl2 | B. | (2)溶液中的SO42-向Cu极定向移动 | ||
| C. | (1)中滴入酚酞试液,C1极附近先变红 | D. | (2)中溶液的PH=1 |
18.某温度下,已知Cl2与NaOH溶液反应产物有NaClO、NaClO3、NaCl,若生成的NaClO与NaClO3的物质的量之比为4:1时,则被氧化与被还原的氯元素的物质的量之比为( )
| A. | 5:1 | B. | 1:5 | C. | 5:9 | D. | 9:5 |
15.下列反应中反应物的总能量比生成物低的是( )
| A. | 灼热的炭与二氧化碳反应 | B. | 铁和稀硫酸的反应 | ||
| C. | 氢氧化钡晶体的粉末和稀硫酸混合 | D. | 木炭在氧气中燃烧 |
19.下列与含氯化合物有关的说法正确的是( )
| A. | HClO是弱酸,所以NaClO是弱电解质 | |
| B. | BaO2是离子化合物,但含有非极性共价键,晶体中阴阳离子个数相等. | |
| C. | HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 | |
| D. | 电解NaCl溶液得到22.4LH2(标准状况),理论上需要转移NA个电子(NA表示阿伏加德罗常数) |
17.对于某些离子的检验及结论一定正确的是( )
| A. | 加入硝酸银溶液生成白色沉淀,再加稀硝酸沉淀不溶解,则溶液中一定有Cl- | |
| B. | 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则溶液中一定有CO${\;}_{3}^{2-}$ | |
| C. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO${\;}_{4}^{2-}$ | |
| D. | 加入氢氧化钠溶液后生成白色沉淀,该白色沉淀迅速变成灰绿色,最终变成红褐色,则溶液中一定含有Fe3+ |