题目内容
7. 一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:2CO(g)+SO2(g)$\stackrel{催化剂}{?}$2CO2(g)+S(l)△H
(1)已知2CO(g)+O2(g)═2CO2(g)△H1=-566kJ/mol
S(l)+O2(g)═SO2(g)△H2=-296kJ/mol,则反应热△H=-270kJ/mol;
(2)一定温度下,向2L恒容密闭容器中通入2molCO和1molSO2,在催化剂作用下发生反应生成CO2(g)和S(l).
①若反应进行到25min时测得CO2的体积分数为0.5.则前25min的反应速率v(CO)=0.024mol.L-1.min-1;
②若反应进行到40min时反应达到平衡状态,此时测得容器中气体的密度比反应前减少了12.8g/L,则CO的物质的量浓度c(CO)=0.2mol.L-1;化学平衡常数K=160;
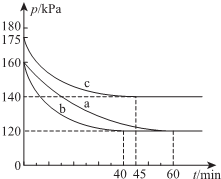
(3)若向2L恒容密闭容器中通入2molCO和1molSO2,反应在不同条件下进行反应:2CO(g)+SO2(g)?2CO2(g)+S(l).反应体系总压强随时间的变化如图所示.
①图中三组实验从反应开始至达到平衡时的反应速率v(CO)由大到小的次序为b>c>a(填实验序号);与实验a相比,c组改变的实验条件可能是升高温度;
②用P0表示开始时总压强,P表示平衡时总压强,用α表示CO的平衡转化率,则α的表达式为a=3-$\frac{3p}{{p}_{0}}$.
分析 (1)已知:①2CO(g)+O2(g)=2CO2(g)△H1=-566kJ•mol-1
②S(l)+O2(g)=SO2(g)△H2=-296kJ•mol-1
根据盖斯定律可知,①-②可得:2CO(g)+SO2(g)?2CO2(g)+S(l),则△H=△H1=-△H2;
(2)一定条件下,向2L恒容密闭容器中通入2molCO和1molSO2,
①设反应进行到25min时转化的CO为xmol,则:
2CO(g)+SO2(g)?2CO2(g)+S(l)
起始量(mol):2 1 0
变化量(mol):x 0.5x x
25min时(mol):2-x 1-0.5x x
根据25min时测得CO2的体积分数列方程计算x,再根据v=$\frac{△c}{△t}$计算v(CO);
②若反应进行到40min时反应达到平衡状态,此时测得容器中气体的密度比反应前减小了12.8g.L-1,则生成S的质量为12.8g/L×2L=25.6g,生成硫的物质的量为$\frac{25.6g}{32g/mol}$=0.8mol,则:
2CO(g)+SO2(g)?2CO2(g)+S(l)
起始量(mol):2 1 0 0
变化量(mol):1.6 0.8 1.6 0.8
平衡时(mol):0.4 0.2 1.6
根据c=$\frac{n}{V}$计算c(CO),平衡常数K=$\frac{{c}^{2}(C{O}_{2})}{{c}^{2}(CO)×c(S{O}_{2})}$;
(3)①恒温恒容下,压强之比等于物质的量之比,单位时间内压强变化越大,说明浓度变化越大,表示的反应速率越快;
a、c开始均通入2molCO和1molSO2,容器的容积相同,而起始时c的压强大于a,物质的量与体积一定,压强与温度呈正比关系;
②用p0表示开始的时候的总压强,p表示平衡时的总压强,a表示CO的平衡转化率,则:
2CO(g)+SO2(g)?2CO2(g)+S(l)
起始量(mol):2 1 0
变化量(mol):2a a 2a
平衡时(mol):2-2a 1-a 2a
再根据压强之比等于物质的量之比计算解答.
解答 解:(1)已知:①2CO(g)+O2(g)=2CO2(g)△H1=-566kJ•mol-1
②S(l)+O2(g)=SO2(g)△H2=-296kJ•mol-1
根据盖斯定律可知,①-②可得:2CO(g)+SO2(g)?2CO2(g)+S(l),则△H=△H1=-△H2=(-566kJ•mol-1)-(-296kJ•mol-1)=-270kJ•mol-1,
故答案为:-270kJ•mol-1;
(2)一定条件下,向2L恒容密闭容器中通入2molCO和1molSO2,
①设反应进行到25min时转化的CO为xmol,则:
2CO(g)+SO2(g)?2CO2(g)+S(l)
起始量(mol):2 1 0
变化量(mol):x 0.5x x
25min时(mol):2-x 1-0.5x x
则$\frac{x}{2-x+1-0.5x+x}$=0.5,解得x=1.2,则v(CO)=$\frac{\frac{1.2mol}{2L}}{25min}$=0.024mol.L-1.min-1,
故答案为:0.024mol.L-1.min-1;
②若反应进行到40min时反应达到平衡状态,此时测得容器中气体的密度比反应前减小了12.8g.L-1,则生成S的质量为12.8g/L×2L=25.6g,生成硫的物质的量为$\frac{25.6g}{32g/mol}$=0.8mol,则:
2CO(g)+SO2(g)?2CO2(g)+S(l)
起始量(mol):2 1 0 0
变化量(mol):1.6 0.8 1.6 0.8
平衡时(mol):0.4 0.2 1.6
则平衡时c(CO)=$\frac{0.4mol}{2L}$=0.2mol.L-1,平衡常数K=$\frac{{c}^{2}(C{O}_{2})}{{c}^{2}(CO)×c(S{O}_{2})}$=$\frac{(\frac{1.6}{2})^{2}}{(\frac{0.4}{2})^{2}×\frac{0.2}{2}}$=160,
故答案为:0.2mol.L-1;160;
(3)①恒温恒容下,压强之比等于物质的量之比,单位时间内压强变化越大,说明浓度变化越大,表示的反应速率越快,a在60min到达平衡,压强变化40 kPa,b在40min到达平衡,压强变化40 kPa,c在45min到达平衡,压强变化35 kPa,可知反应速率:b>c>a;
a、c开始均通入2molCO和1molSO2,容器的容积相同,而起始时c的压强大于a,物质的量与体积一定,压强与温度呈正比关系,故c组改变的实验条件可能是:升高温度,
故答案为:b>c>a;升高温度;
②用p0表示开始的时候的总压强,p表示平衡时的总压强,a表示CO的平衡转化率,则:
2CO(g)+SO2(g)?2CO2(g)+S(l)
起始量(mol):2 1 0
变化量(mol):2a a 2a
平衡时(mol):2-2a 1-a 2a
压强之比等于物质的量之比,则p0:p=3:(2-2a+1-a+2a),整理可得a=3-$\frac{3p}{{p}_{0}}$,
故答案为:a=3-$\frac{3p}{{p}_{0}}$.
点评 本题综合考查化学平衡的有关计算、化学平衡影响因素、平衡常数、反应热计算等知识,为高考常见题型,侧重于学生的分析、计算能力的考查,注意掌握化学平衡计算中三段式的应用,难度中等.

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案| A. | 98.32kJ | B. | 196.64kJ/mol | C. | <196.64kJ | D. | >196.64kJ |
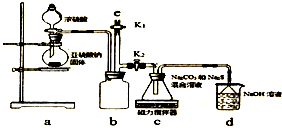
已知:Na2S2O3在酸性溶液中不能稳定存在.有关物质的溶解度随温度变化曲线如图2所示.某研究小组设计了制备Na2S2O3•5H2O的装置图(如图1).
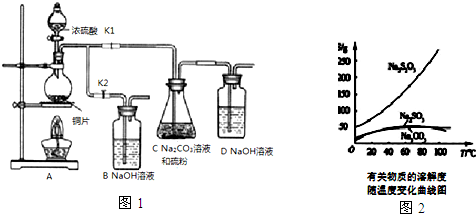
部分操作步骤如下:
①打开K1,关闭K2,向圆底烧瓶中加入足量浓硫酸,加热.
②C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.当C中溶液的pH接近7时,即停止C中的反应,停止加热
③过滤C中的混合液,并将滤液进行处理,得到产品.
(1)步骤①中,圆底烧瓶中发生反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)步骤②中,“当C中溶液的pH接近7时即停止C中的反应”的原因是Na2S2O3在酸性溶液中不能稳定存在.“停止C中的反应”的操作是打开K2,关闭K1.
(3)步骤③中,“过滤”用到的玻璃仪器是烧杯、漏斗、玻璃棒(填仪器名称).将滤液进行处理过程是将滤液经过加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.
依据反应2S2O32-+I2→S4O62-+2I-,可用I2的标准溶液测定产品的纯度.取5.5g产品配制成100mL溶液.取10mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,相关数据记录如表所示.
| 编号 | 1 | 2 | 3 | 4 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.99 | 19.98 | 17.13 | 20.03 |
(5)Na2S2O3•5H2O在产品中的质量分数是90.2%.(计算结果请用百分数表示并保留1位小数)(Na2S2O3•5H2O的式量为248)
| A. | 化学反应必然伴随着能量的变化 | |
| B. | 能量转化的途径不同时,体系包含的总能量不同 | |
| C. | 放热反应指生成物的总能量高于反应物的总能量 | |
| D. | 吸热反应不加热就不会发生 |
 已知H2C2O4为二元中强酸.某化学兴趣小组为测定含Na2SO4、NaHC2O4和H2C2O4•2H2O的试样中各物质的质量分数,进行了如下实验:
已知H2C2O4为二元中强酸.某化学兴趣小组为测定含Na2SO4、NaHC2O4和H2C2O4•2H2O的试样中各物质的质量分数,进行了如下实验: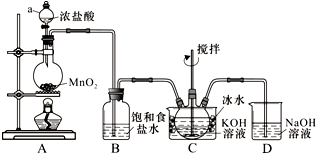
 天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染.
天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染.