题目内容
12.现有下列十种物质:①氯气 ②小苏打 ③固体纯碱 ④二氧化硫 ⑤蔗糖 ⑥氢氧化钾 ⑦氢氧化铁胶体 ⑧氨水 ⑨空气 ⑩浓硫酸(1)上述十种物质中,属于电解质的有②③⑥,属于非电解质的有④⑤.(填序号)
(2)将①与④按1:1的体积比通入水中,反应的化学方程式为Cl2+SO2+2H2O=2HCl+H2SO4.
(3)除去③中少量②的操作是加热,化学方程式为2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(4)现在⑤中加入⑩时,观察到蔗糖变黑、体积膨胀并放出刺激性气味气体的现象,体现了⑩的脱水性和强氧化性性质,放出刺激性气味气体发生反应的化学方程式是C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O.
分析 (1)电解质:在水溶液中或熔融状态下能够导电的化合物;非电解质:在熔融状态和水溶液中都不能导电的化合物;
(2)①氯气 和④二氧化硫通入水中发生氧化还原反应生成硫酸和盐酸;
(3)根据碳酸钠加热不分解,碳酸氢钠加热分解得到碳酸钠、水、二氧化碳来解答;
(4)⑤蔗糖中加入⑩浓硫酸时,观察到蔗糖变黑、体积膨胀并放出刺激性气味气体的现象,说明浓硫酸具有脱水性和强氧化性,反应生成刺激下气味气体是碳和浓硫酸反应生成.
解答 解:(1)①氯气在水溶液中能导电,氯气为单质既不是电解质也不是非电解质;
②小苏打NaHCO3在水溶液或者熔融状态下能够导电,是电解质;
③固体纯碱在水溶液或者熔融状态下能够导电,是电解质;
④二氧化硫不能电离属于非电解质;
⑤蔗糖在水溶液和熔融状态下都不能够导电,是非电解质;
⑥氢氧化钾在水溶液或者熔融状态下能够导电,是电解质;
⑦氢氧化铁胶体属于混合物 既不是电解质也不是非电解质;
⑧氨水属于混合物 既不是电解质也不是非电解质;
⑨空气属于混合物 既不是电解质也不是非电解质;
⑩浓硫酸属于混合物 既不是电解质也不是非电解质;
故属于电解质的是:②③⑥,非电解质的有:④⑤;
故答案为:②③⑥;④⑤;
(2)①氯气 和④二氧化硫通入水中发生氧化还原反应生成硫酸和盐酸,反应的化学方程式为:Cl2+SO2+2H2O=2HCl+H2SO4,
故答案为:Cl2+SO2+2H2O=2HCl+H2SO4;
(3)根据碳酸钠加热不分解,碳酸氢钠加热分解得到碳酸钠、水、二氧化碳,所以除去固体纯碱中少量小苏打的操作是加热,方程式为:2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,
故答案为:加热;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(4)⑤蔗糖中加入⑩浓硫酸时,观察到蔗糖变黑、体积膨胀并放出刺激性气味气体的现象,说明浓硫酸具有脱水性和强氧化性,反应生成刺激下气味气体是碳和浓硫酸反应生成,反应的化学方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ 2SO2↑+CO2↑+2H2O,
故答案为:脱水性和强氧化性;C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ 2SO2↑+CO2↑+2H2O.
点评 本题考查了物质导电的条件,电解质和非电解质的概念,离子方程式书写,物质的量有关计算等,题目综合性强,浓硫酸性质是本题的难点,题目难度中等.

①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂
②用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
③草木灰与铵态氮肥不能混合施用
④实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤加热蒸干AlCl3溶液得到Al(OH)3固体
⑥HF水溶液不能用玻璃试剂瓶盛装.
| A. | ①②③ | B. | ②③④ | C. | ①②③④⑤ | D. | ①②③④⑤⑥ |
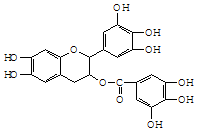 已知绿茶中含有EGCG,该物质具有抗癌作用,EGCG的结构简式如图所示,有关说法不正确的是( )
已知绿茶中含有EGCG,该物质具有抗癌作用,EGCG的结构简式如图所示,有关说法不正确的是( )| A. | 1molEGCG最多可与9mol H2发生加成反应 | |
| B. | 1molEGCG最多可与含6mol Br2的浓溴水反应 | |
| C. | EGCG在空气中易被氧化 | |
| D. | EGCG能与碳酸氢钠溶液反应 |
| A. | 明矾水解形成的Al(OH)3胶体能杀菌消毒,可用于水的净化 | |
| B. | 镀锡的铁制品比镀锌的铁制品耐腐蚀 | |
| C. | pH=6的某溶液一定呈酸性 | |
| D. | 二次电池充电时,电池上标有“+”的电极应与外接电源的正极相连 |
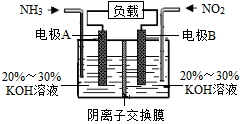 利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示.下列说法正确的是( )
利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示.下列说法正确的是( )| A. | 电极B为负极 | |
| B. | 电极A的反应式为2NH3-6e-+6OH-=N2+6H2O | |
| C. | 溶液中OH-通过阴离子交换膜从左向右迁移 | |
| D. | 当有4.48LNO2(标准状况下)被处理时,转移的电子为0.4mol |
| A. | 标准状况下,22.4L酒精中含有的分子数目为NA | |
| B. | 常温常压下,l.mol/L盐酸中含有的氯离子数目为NA | |
| C. | 常温常压下,24gO2和24gO3含有的氧原子数目都为1.5NA | |
| D. | 标准状况下,2.24L氯气与足量NaOH溶液反应转移的电子数为0.2NA |
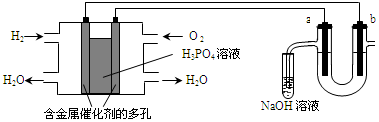 用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a,b为石墨电极).下列说法中正确的是( )
用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a,b为石墨电极).下列说法中正确的是( )| A. | 电池工作时,正极反应式为O2+2H2O+4e-═4OH | |
| B. | 电解时,电子流动路径是负极→外电路→阴极→溶液→阳极→正极 | |
| C. | 试管中NaOH溶液用来吸收电解时产生的Cl2 | |
| D. | 当电池中消耗2.24L(标准情况下)H2时,b极周围会产生0.021mol气体 |
 NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题: