题目内容
7.化学家制造出一种物质“干水”,其每个颗粒含水95%,外层是沙质硅,干水吸收CO2的能力比普通水高三倍.下列说法正确的是( )| A. | 干水是纯净物 | B. | 干水和干冰是同一种物质 | ||
| C. | 干水中的水分子不再运动 | D. | 用干水能更好地吸收CO2 |
分析 由信息:“干水”,其每个颗粒含水95%,外层是沙质硅,得出此物质是混合物,能很好的吸收二氧化碳,据此解答即可.
解答 解:A.“干水”,其每个颗粒含水95%,外层是沙质硅,属于混合物,故A错误;
B.干冰是固体二氧化碳,两者不是一种物质,故B错误;
C.水分子是不断运动着的,故C错误;
D.由信息可知,干水吸收CO2的能力比普通水高三倍,故D正确,故选D.
点评 本题是一道信息给与题,题目较为新颖,抓住所给信息的关键(“干水”,其每个颗粒含水95%,外层是沙质硅,干水吸收CO2的能力比普通水高三倍)是解决本题的关键,难度不大.

练习册系列答案
相关题目
18.2molA与2molB混合于2L的密闭容器中,发生如下反应:2A(g)+3B(g)?2C(g)+zD(g),2s后A的转化率为50%,测得v(D)=0.25mol•L-1•s-1,下列推断不正确的是( )
| A. | z=2 | B. | 2s后,容器内的压强是初始的$\frac{7}{8}$倍 | ||
| C. | 2s时C的体积分数为$\frac{2}{7}$ | D. | 2s后,B的浓度为0.5mol/L |
15.多硫化钠Na 2S x(x≥2)在NaOH溶液中可被NaClO氧化成Na2SO4,而NaClO被还原成NaCl,反应中Na2Sx与NaClO的物质的量之比为1:16.Na2Sx在结构上与Na2Sx类似.则下列有关说法正确的是( )
| A. | 该反应中Na2Sx是氧化剂,NaClO是还原剂 | |
| B. | Na2Sx含有离子键和极性共价键 | |
| C. | 1molNa2Sx参加反应,有32mol电子转移 | |
| D. | Na2Sx中的X数值为2 |
2.将两个铂电极放置在KOH溶液中,然后分别通入CH4 和O2,即可产生电流,称为燃料电池,下面叙述正确的是( )
| A. | 通入CH4的电极为正极 | |
| B. | 通入CH4的电极反应为:CH4+10OH-→CO32-+7H2O+8e- | |
| C. | 通入O2的电极为负极 | |
| D. | 放电时溶液中阴离子向正极移动 |
12.下列各组物质相互混合,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入FeCl3溶液 ②过量NaOH溶液和明矾溶液混合
③镁铝合金投入足量稀盐酸 ④Na2O2投入FeCl2溶液.
①金属钠投入FeCl3溶液 ②过量NaOH溶液和明矾溶液混合
③镁铝合金投入足量稀盐酸 ④Na2O2投入FeCl2溶液.
| A. | ① | B. | ③ | C. | ②③ | D. | ①④ |
19.常温时,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
| A. | 某HCl溶液的pH值为2,则溶液中由水电离的c(H+)=10-2mol•L-1 | |
| B. | 0.1 mol•L-1的KHA溶液,其pH=10,c(K+)>c(A2-)>c(HA-)>c(OH-) | |
| C. | 等体积、等物质的量浓度的Na2CO3溶液与NaHCO3溶液混合:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) | |
| D. | 将0.2 mol•L-1的某一元酸HA溶液和0.1 mol•L-1NaOH溶液等体积混合后溶液pH>7,则反应后的混合液:c(HA)>C(Na+)>c(A-) |
16.设阿伏加德罗常数的数值为NA,下列说法不正确的是( )
| A. | 46 g的NO2和N2O4混合气体含有的原子数为3NA | |
| B. | 1 mol Na2O2与足量H2O反应,转移的电子数为NA | |
| C. | 物质的量浓度为0.5 mol/L MgCl2溶液,含有Cl-离子数为NA | |
| D. | 2.7g铝与足量的盐酸或氢氧化钠溶液反应,生成H2的分子数均为0.15NA |
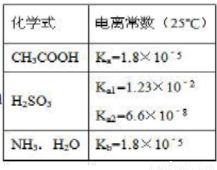
 OOH) =c (CH3COO-
OOH) =c (CH3COO- ) +2c (OH-)
) +2c (OH-)