题目内容
实验室里迅速制备少量氯气可利用如下反应:2KMnO4+16HCl(浓)═2KCl+2MnCl2↑+5Cl2↑+8H2O,此反应不需加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高.
(1)用单线桥表示该反应的电子转移情况:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(2)该反应中,氧化剂是 ,氧化产物是 ,当有1mol电子转移时,产生的氯气在标准状况下的体积为
(3)结合此反应原理,联系实际思考,实验室处理含MnO4-的废液时,要特别注意的问题是 .
(1)用单线桥表示该反应的电子转移情况:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(2)该反应中,氧化剂是
(3)结合此反应原理,联系实际思考,实验室处理含MnO4-的废液时,要特别注意的问题是
考点:氧化还原反应的电子转移数目计算,氧化还原反应
专题:
分析:(1)反应中,化合价升高元素是氯元素,失电子,化合价降低元素是锰元素,得到电子,化合价升高数=化合价降低数=转移电子数=10,单线桥表,反应中电子转移的方向和数目为:
(2)所含元素化合价升高的是还原剂,所含元素化合价降低的是氧化剂;
(3)因为MnO4-具有强氧化性,会与Cl-发生氧化还原反应生成有毒的Cl2.
(2)所含元素化合价升高的是还原剂,所含元素化合价降低的是氧化剂;
(3)因为MnO4-具有强氧化性,会与Cl-发生氧化还原反应生成有毒的Cl2.
解答:
解:(1)反应中,化合价升高元素是氯元素,失电子,化合价降低元素是锰元素,得到电子,化合价升高数=化合价降低数=转移电子数=10,单线桥表,反应中电子转移的方向和数目为:
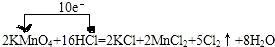 ;
;
故答案为: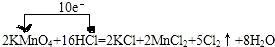 ;
;
(2)2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O反应中,高锰酸钾中锰元素化合价降低,所以高锰酸钾做氧化剂,氯化氢中氯元素化合价升高,氯化氢为还原剂,生成5mol氯气,转移10mol电子,所以转移1mol电子时,生成0.5mol氯气,标况下体积为0.5mol×22.4L/mol=11.2L;
故答案为:KMnO4;HCl;11.2L;
(3)MnO4-具有强氧化性,会与Cl-发生氧化还原反应生成有毒的Cl2,造成空气污染;
故答案为:MnO4-具有强氧化性,会与Cl-发生氧化还原反应生成有毒的Cl2.
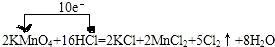 ;
;故答案为:
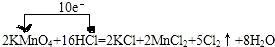 ;
;(2)2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O反应中,高锰酸钾中锰元素化合价降低,所以高锰酸钾做氧化剂,氯化氢中氯元素化合价升高,氯化氢为还原剂,生成5mol氯气,转移10mol电子,所以转移1mol电子时,生成0.5mol氯气,标况下体积为0.5mol×22.4L/mol=11.2L;
故答案为:KMnO4;HCl;11.2L;
(3)MnO4-具有强氧化性,会与Cl-发生氧化还原反应生成有毒的Cl2,造成空气污染;
故答案为:MnO4-具有强氧化性,会与Cl-发生氧化还原反应生成有毒的Cl2.
点评:本题考查了氧化还原反应的相关概念和计算,明确氧化还原反应的实质是解题关键,注意分析化合价判断电子的转移数目,依据方程式计算,题目难度不大.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
利用蛋白质的变性可以为我们的日常生活,医疗卫生服务.下列实例利用了蛋白质的变性的是①利用过氧乙酸对环境、物品进行消毒;②利用高温、紫外线对医疗器械进行消毒;③蒸煮鸡蛋食用;④松花蛋的腌制;⑤用蛋白质灌服重金属中毒的病人.( )
| A、全部 | B、①②③④ |
| C、①②③ | D、①②. |
含有0.20mol碳酸钠的溶液和200mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
| A、2.0mol/L |
| B、1.5 mol/L |
| C、0.18 mol/L |
| D、0.24mol/L |
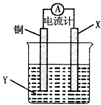 根据反应为 2Cu+O2+CO2+H2O=Cu2(OH)2CO3,设计如图所示原电池,下列说法错误的是( )
根据反应为 2Cu+O2+CO2+H2O=Cu2(OH)2CO3,设计如图所示原电池,下列说法错误的是( )| A、X可以是银或石墨 |
| B、电子从铜电极经外电路流向X电极 |
| C、Y是硫酸铜溶液 |
| D、X极上的电极反应式为 O2+2H2O+4e-=4OH- |
某种气体的摩尔质量为M g?mol-1,将标况下的该气体V L溶解在1000g水中,该气体不与水反应,所得溶液密度为ρ g?cm-3,则所得溶液中溶质的物质的量浓度为( ) mol?L-1.
A、
| ||
B、
| ||
C、
| ||
D、
|
下列电离方程式正确的是( )
| A、CH3COOH=CH3COO-+H+ |
| B、H2SO4=2H++SO42- |
| C、Ba(OH)2=Ba2++(OH-)2 |
| D、KHCO3=K++H++CO32- |