题目内容
19.下列实验操作或对实验事实的叙述中存在错误的是( )| A. | 用50mL酸式滴定管准确量取23.20mL酸性KMnO4溶液,放入锥形瓶中待用 | |
| B. | 制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 | |
| C. | 使用pH试纸测定溶液pH时先润湿,则测得溶液的pH会发生变化 | |
| D. | 用惰性电极电解NaCl溶液一段时间后,再加入盐酸可使溶液与原溶液完全一样 |
分析 A.滴定管精确到0.01mL,酸性高锰酸钾溶液具有强氧化性,需要用酸式滴定管量取;
B.盐酸具有挥发性,加热过程促进了水解,无法通过蒸干的方法制备AlCl3、FeCl3、CuCl2;
C.使用pH试纸时不能湿润,否则待测液被稀释,影响测定结果;
D.电解氯化钠时,阳极产生氯气,阴极产生氢气.
解答 解:A.滴定管精确到0.01,可量取25.00mL酸性KMnO4溶液,故A正确;
B.因盐酸为挥发性酸,制备AlCl3、FeCl3、CuCl2发生水解生成盐酸,故不能采用将溶液直接蒸干的方法制备,故B正确;
C.使用pH试纸测定溶液pH时先润湿,则待测液被稀释,导致测得溶液的pH会发生变化,故C正确;
D.电解氯化钠时,阳极产生氯气,阴极产生氢气,所以应加氯化氢让电解质溶液复原,故D错误;
故选D.
点评 本题考查较为综合,涉及物质制备、中和滴定、电解等知识,侧重于学生的分析能力和实验能力的考查,为高考常见题型,题目难度不大,明确化学实验基本操作方法为解答结构,注意掌握电解原理、盐的水解原理及应用,试题培养了学生的化学实验能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.在光照的条件下,将1mol甲烷与一定量的氯气充分混合,经过一段时间,甲烷和氯气均无剩余,生成一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳和氯化氢,若已知生成的二氯甲烷、三氯甲烷、四氯化碳的物质的量分别为a mol,b mol,c mol,该反应中消耗的氯气的物质的量是( )
| A. | (1-a-b-c)mol | B. | (1+a+2b+3c) mol | C. | (2a+3b+4c)mol | D. | (a+b+c)mol |
4.已知下列两个热化学方程式
2H2O(l)=2H2(g)+O2(g);△H=+571.6kJ
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H=-2220.0kJ
实验测得氢气和丙烷的混和气体共5mol完全燃烧时放热3847kJ,则混和气体中氢气与丙烷的体积比是( )
2H2O(l)=2H2(g)+O2(g);△H=+571.6kJ
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H=-2220.0kJ
实验测得氢气和丙烷的混和气体共5mol完全燃烧时放热3847kJ,则混和气体中氢气与丙烷的体积比是( )
| A. | 1:3 | B. | 3:1 | C. | 1:4 | D. | 1:1 |
11.下面有关Na2CO3与NaHCO3的叙述错误的是( )
| A. | Na2CO3遇少量酸可转化为NaHCO3 | |
| B. | 在水中的溶解度Na2CO3比NaHCO3大 | |
| C. | 与同浓度的硫酸反应时,Na2CO3比NaHCO3剧烈 | |
| D. | NaHCO3比Na2CO3的碱性弱 |
 CH3OH(g) △H。下表所列数据是该反应在不同温度下的化学平衡常数(K)
CH3OH(g) △H。下表所列数据是该反应在不同温度下的化学平衡常数(K)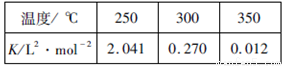

 质的量浓度随时间变化的趋势示意图(其他条件不变,曲
质的量浓度随时间变化的趋势示意图(其他条件不变,曲 线上必须标明氢气、甲醇)。
线上必须标明氢气、甲醇)。 电极反应式________________________。
电极反应式________________________。 为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E是原子核外电子排布未成对电子数最多的元素,ECl
为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E是原子核外电子排布未成对电子数最多的元素,ECl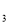 能与B、C的氢化物形成六配位的配合物,且B、C的氢化物物质
能与B、C的氢化物形成六配位的配合物,且B、C的氢化物物质 的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示) 化学方程式是 。
化学方程式是 。