题目内容
下列递变规律正确的是( )
| A、HClO4、H2SO4、H3PO4的酸性依次增强 |
| B、P、S、Cl最高正价依次降低 |
| C、钠、镁、铝的还原性依次减弱 |
| D、HCl、HBr、HI的稳定性依次增强 |
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A、比较最高价含氧酸的酸性可以通过比较元素的非金属性得出结论;
B、元素的最高正价=主族序数;
C、元素的金属性逐渐变弱,单质的还原性也逐渐变弱;
D、非金属性越强,和H2化合越容易,得到的气态氢化物越稳定.
B、元素的最高正价=主族序数;
C、元素的金属性逐渐变弱,单质的还原性也逐渐变弱;
D、非金属性越强,和H2化合越容易,得到的气态氢化物越稳定.
解答:
解:A、元素的非金属性越强,最高检含氧酸的酸性越强,而非金属性Cl>S>P,故酸性HClO4、H2SO4、H3PO4逐渐减弱,故A错误;
B、元素的最高正价=主族序数,故P、S、Cl最高正价依次升高,故B错误;
C、在金属活动性顺序表中,从左到右,元素的金属性逐渐变弱,单质的还原性也逐渐变弱,故C正确;
D、非金属性越强,和H2化合越容易,得到的气态氢化物越稳定.第ⅤⅡA族的元素,从上而下,元素的非金属性越来越弱,故气态氢化物的稳定性逐渐减弱,故D错误.
故选C.
B、元素的最高正价=主族序数,故P、S、Cl最高正价依次升高,故B错误;
C、在金属活动性顺序表中,从左到右,元素的金属性逐渐变弱,单质的还原性也逐渐变弱,故C正确;
D、非金属性越强,和H2化合越容易,得到的气态氢化物越稳定.第ⅤⅡA族的元素,从上而下,元素的非金属性越来越弱,故气态氢化物的稳定性逐渐减弱,故D错误.
故选C.
点评:本题考查了元素的非金属性的周期性变化导致的最高价含氧酸的酸性、气态氢化物的稳定性、金属单质的还原性等的变化规律,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各物质所含原子数目,按由多到少顺序排列的是( )
①11.2L NH3 ②标准状况下,4g He
③4℃时的9mL水 ④0.2mol H3PO4.
①11.2L NH3 ②标准状况下,4g He
③4℃时的9mL水 ④0.2mol H3PO4.
| A、①④③② | B、④③②① |
| C、②③④① | D、①④②③ |
现已知O3分子为V字形结构,O3在水中的溶解度和O2比较( )
| A、O3在水中的溶解度和O2一样 |
| B、O3在水中的溶解度比O2小 |
| C、O3在水中的溶解度比O2要大 |
| D、没办法比较 |
下列元素属于第三周期的是( )
| A、S | B、H | C、O | D、N |
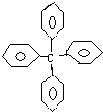 甲烷分子中的4个氢原子全部被苯基取代,可得分子的结构为,对该分子的叙述不正确的是( )
甲烷分子中的4个氢原子全部被苯基取代,可得分子的结构为,对该分子的叙述不正确的是( )| A、分子式为C25H20 |
| B、此物质不是苯的同系物 |
| C、此物质属于芳香烃 |
| D、该分子中所有原子有可能处于同一平面上 |
下列每组分别给出了两个量,其中可以组成一个物质的量公式的组合是( )
| ① | ② | ③ | ④ | ⑤ |
| 物质的微粒数 | 固体体积 | 标况下气体摩尔体积 | 溶质的质量分数 | 非标况下物质的质量 |
| 阿伏加德罗常数 | 固体密度 | 标况下气体体积 | 溶液的体积 | 物质的摩尔质量 |
| A、①③⑤ | B、②③④ |
| C、①④⑤ | D、①③④ |
下列离子方程式书写正确的是( )
| A、标况下2.24L CO2通入1 mol?L-1100mL氢氧化钠溶液中:CO2+OH-=HCO3- |
| B、硝酸铝溶液中加入过量氨水:Al3++4NH3?H2O=[Al(OH)4]-+4 NH4+ |
| C、稀硫酸中加入铁粉:2Fe+6H+═2Fe3++3H2↑ |
| D、等物质的量的NH4HCO3与NaOH在溶液中反应:NH4++HCO3-+2OH-=CO32-+NH3↑+2H2O |