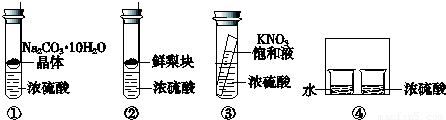
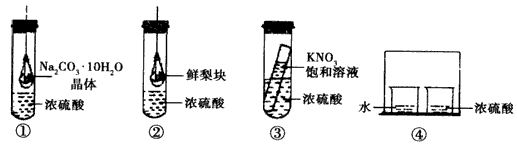
题目内容
某同学为探究浓硫酸的性质,设计了以下实验装置图。检查好装置的气密性后,向烧瓶A中加入过量的铁粉、炭粉,再滴加浓硫酸。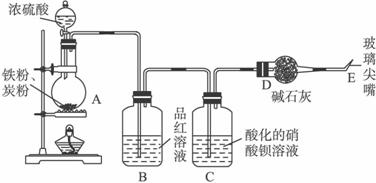
(1)在未点燃酒精灯前,该同学观察到B中没有出现明显的现象,这是因为_____________;点燃酒精灯后,烧瓶内可能发生的化学反应为:
2Fe+6H2SO4(浓)![]() Fe2(SO4)3+3SO2↑+6H2O
Fe2(SO4)3+3SO2↑+6H2O
C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
随着反应的进行,还可能发生其他反应,试写出其中两个反应的离子反应方程式:________
____________________________________________________________________。
(2)当反应进行一段时间后,在C瓶中观察到有白色沉淀产生,该沉淀是_______(填化学式),在点燃E处产生的气体之前要先进行验纯,请简述操作及有关现象______________。
(3)在烧瓶中加入碳粉,可以使E处产生气体的速率加快,原因是:________________。
(4)反应结束后,安装好过滤装置。先用少量热水通过过滤器,以提高它的温度,然后将烧瓶中的溶液趁热过滤。将滤液转入试管中,用橡皮塞塞住管口,静置、冷却,可以看到硫酸亚铁晶体在试管中结晶析出。将析出的晶体过滤、干燥、称重,得硫酸亚铁晶体
已知:硫酸亚铁晶体在受热时发生的反应为:
2FeSO4·xH2O![]() Fe2O3+SO2↑+SO3↑+2xH2O。请回答:
Fe2O3+SO2↑+SO3↑+2xH2O。请回答:
①提高过滤器温度的目的是__________________;
②用橡皮塞塞住管口是为了_________________;
③求该晶体中所含结晶水的个数(要求写出计算过程)。
(1)常温下,Fe遇浓硫酸钝化,而C不与浓硫酸反应。2Fe3++Fe====3Fe2+; Fe+2H+====Fe2++H2↑。(其他合理答案也可)(2)BaSO4,用一只小试管收集从玻璃尖嘴管排出的气体,收集满后用大拇指堵住试管口,靠近酒精灯火焰,移开手指,如果听到尖锐的爆鸣声说明气体不纯,如果听到噗的一声,证明气体已纯净,可以进行点燃。(3)铁与碳在硫酸中形成了原电池,加快反应速率。(4)①防止溶液冷却,晶体在漏斗中析出;②防止空气进入,使亚铁离子氧化。
③2FeSO4·xH2O![]() Fe2O3+SO2↑+SO3↑+2xH2O
Fe2O3+SO2↑+SO3↑+2xH2O
2mol
![]()
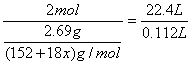
x=6.5。
解析:(1)Fe遇冷的浓H2SO4钝化,炭与冷的浓H2SO4不反应。当硫酸浓度变稀后,溶液中的Fe3+、H+均能与Fe反应,2Fe3++Fe====3Fe2+,2H++Fe====H2↑+Fe2+。(2)反应一段时间后,进入C中的SO2与Ba(NO3)2溶液反应生成BaSO4沉淀。检验气体是否纯净的操作是:用一只小试管收集从玻璃尖嘴管排出的气体,收集满后用大拇指堵住试管口,靠近酒精灯火焰,移开手指,如果听到尖锐的爆鸣声说明气体不纯,如果听到噗的一声,证明气体已纯净,可以点燃。(3)加入碳粉后形成了以Fe为负极的原电池,生成H2的反应速率加快。(4)①分析不提高过滤器温度会出现的结果,提高过滤器温度的目的是为了防止过滤时FeSO4在漏斗中结晶析出。②分析不用橡皮塞塞住管口是为了防止空气中的O2将FeSO4氧化。③SO3在标准状况下为固态。
FeSO4·xH2O—![]() SO2↑,
SO2↑,
(152+18x) g
解得x=6.5。